
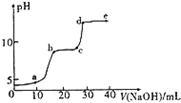
 ij�о���ѧϰС����̽���ں�Mg2+��Al3+�Ļ����Һ�еμ�NaOH��Һʱ������������������Ĺ��̣�
ij�о���ѧϰС����̽���ں�Mg2+��Al3+�Ļ����Һ�еμ�NaOH��Һʱ������������������Ĺ��̣�| �ϴ������ڵĺ�����Ԫ�ص����� | ���鷽�� |
���� ��ͼ���֪��pH�仯��������Ҫԭ��ӦΪ������Mg��OH��2����������OH-������Al��OH��3��������OH-�� Al��OH��3�����ܽ⣬����OH-���ֿ��ܣ�������һ��Ϊ���ֿ��ܣ�Ӧ�� Al��OH��3��Mg��OH��2���ߵ��ܽ���йأ�
��1���ζ��ܵ���Һ�����ȷ��0.01ml����ʽ�ζ�����������ȷ���Ƽ���NaOH��Һ�������
��2������Mg��OH��2����������OH-������Al��OH��3��������OH-��
��3�����ݷ�����֪��PH�仯��������Ҫԭ��ӦΪ������Mg��OH��2����������OH-������Al��OH��3��������OH-�� Al��OH��3�����ܽ⣬����OH-���ֿ��ܣ����Ʋ�1����ʵ�������b��c֮������Mg��OH��2����������OH-����a��֮ǰӦ���Dz������������ķ�Ӧ��
��4���������Ϸ����ó���e��ǰ�ķ�ӦΪAl��OH��3+OH-�TAl��OH��4-������e�����Һ�нϴ������ڵĺ�����Ԫ�ص�����Ϊ�����Ӻ�Al��OH��4-���ӣ���ɫ��Ӧ���������Ӵ��ڣ�Al��OH��4-���Ӻ��������ᷴӦ���������������������������ʹ���������ܽ⣮
��� �⣺��1����ȷ���Ƽ���NaOH��Һ�������Ӧ�þ�ȷ��0.01ml�ĵζ��ܣ���NaOH�ʼ��ԣ���ѡ�ü�ʽ�ζ��ܣ��ʴ�Ϊ����ʽ�ζ��ܣ�
��2����ͼ���֪��PH�仯��������Ҫԭ��ӦΪ������Mg��OH��2����������OH-������Al��OH��3��������OH-�� Al��OH��3�����ܽ⣬����OH-���ֿ��ܣ���һ�Σ�a��ǰ��Ӧ�������ɳ��������˵���ȥ���������ƣ�������Ϊ�����ɰ�ɫ�����������࣬
�ʴ�Ϊ�����ɰ�ɫ�����������ࣻ
��3�����ݷ�����֪��PH�仯��������Ҫԭ��ӦΪ������Mg��OH��2����������OH-������Al��OH��3��������OH-�� Al��OH��3�����ܽ⣬����OH-���ֿ��ܣ����Ʋ�1����ʵ�������b��c֮������Mg��OH��2����������OH-����a��֮ǰӦ���Dz������������ķ�Ӧ�����Է�Ӧ�����ӷ���ʽΪAl3++3OH-�TAl��OH��3�����ݴ�˵���ڼ�����Һ�������ӱ�þ���Ӹ��׳���������Al��OH��3��Mg��OH��2��������ˮ��
�ʴ𰸣�����Al��OH��3��������OH-��Al��OH��3�����ܽ⣬����OH-��Al3++3OH-�TAl��OH��3����Al��OH��3��Mg��OH��2��������ˮ��
��4���������Ϸ����ó���e��ǰ�ķ�ӦΪAl��OH��3+OH-�TAl��OH��4-������e�����Һ�нϴ������ڵĺ�����Ԫ�ص�����Ϊ�����Ӻ�Al��OH��4-���ӣ����������ӿ�����������ɫ��Ӧ������ɫ��Ӧ�ʻ�ɫ֤������Ԫ�أ��ýྻ�IJ�˿պȡ��������Һ�ھƾ��ƻ��������գ�������ʻ�ɫ����������Na+��Al��OH��4-���Ӻ����ᷴӦ���������������������������ʹ�����ܽ⣬ȡ��������Һ���Թ��У��μ����ᣬ������ɫ�������������ʱ���������ܽ⣬
�ʴ�Ϊ��
| �ϴ������ڵĺ�����Ԫ�ص����� | ���鷽�� |
| Na+ | �ýྻ�IJ�˿պȡ��������Һ�ھƾ��ƻ��������գ�������ʻ�ɫ����������Na+ |
| [Al��OH��4]- | ȡ��������Һ���Թ��У��μ����ᣬ������ɫ�������������ʱ���������ܽ� |
���� ���⿼����ѧ������ͼ�������Ӧ���̵�����������ؼ���������Ϥ�й�þ�������ʣ���Ŀ�Ѷ��еȣ������ڿ���ѧ���ķ���������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
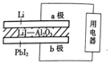 ij﮵�����LiI-Al2O3����Ϊ����ʴ������ӣ�������ṹʾ��ͼ���£�����ܷ�Ӧ�ɱ�ʾΪ��2Li+PbI2�T2LiI+Pb������˵����ȷ���ǣ�������
ij﮵�����LiI-Al2O3����Ϊ����ʴ������ӣ�������ṹʾ��ͼ���£�����ܷ�Ӧ�ɱ�ʾΪ��2Li+PbI2�T2LiI+Pb������˵����ȷ���ǣ�������| A�� | ������b�����õ�������a�� | |
| B�� | I-��a��ͨ���������ʴ��ݵ�b�� | |
| C�� | b���ϵĵ缫��ӦʽΪ��PbI2+2e-�TPb+2I- | |
| D�� | b����������1.27gʱ��a��ת�Ƶĵ�����ԼΪ6.02��1021 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��a����Ԫ�����γɶ���ԭ�Ӹ���֮��Ϊ1��1�Ļ����� | |
| B�� | Ԫ��b�ĵ��ʲ�������ˮ�Ҵ���Ӧ | |
| C�� | Ԫ��c��Ԫ��d�γɵĻ������ˮ��Һ�ʼ��� | |
| D�� | Ԫ��a��Ԫ��d�γɵĻ������п϶����м��Լ��������ܺ��зǼ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 5.6 g��������ϡ���ᷴӦ��ת�Ƶ��ӵ���ĿΪ0.2 NA | |
| B�� | ��״���£�22.4 L���ȼ���ķ�����ԼΪNA | |
| C�� | 8.8g���������к����õ��Ӷ���Ϊ1.4 NA | |
| D�� | 1 L 0.1 mol•L-1�Ȼ�ͭ��Һ��ͭ������Ϊ0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ����Ʊ���ȩ��ͬʱ�ܻ�õ��ܣ����ܷ�ӦΪ��2CH2�TCH2+O2��2CH3CHO�������й�˵������ȷ���ǣ�������
��ϩ����������ȩ����Ƴ���ͼ��ʾ��ȼ�ϵ�أ����Ʊ���ȩ��ͬʱ�ܻ�õ��ܣ����ܷ�ӦΪ��2CH2�TCH2+O2��2CH3CHO�������й�˵������ȷ���ǣ�������| A�� | �õ�ؿɽ���ѧ��ת��Ϊ���� | |
| B�� | ÿ��0.1 mol O2��Ӧ����Ǩ��0.4 mol H+ | |
| C�� | ������ӦʽΪ��CH2=CH2-2e-+2OH-�TCH3CHO+H2O | |
| D�� | ��������Һ��pH��С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
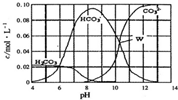 25��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1L ����Һ����Һ�в�������pH�Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ���ǣ�������
25��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1L ����Һ����Һ�в�������pH�Ĺ�ϵ��ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ���ǣ�������| A�� | W����ʾ����Һ�У�c��Na+��+c��H+��=4c��CO32-��+c��OH-��+c��Cl-�� | |
| B�� | pH=4����Һ�У�c��H2CO3��+c��HCO3-��+c��CO32-��=0.1 mol/L | |
| C�� | pH=8����Һ�У�c��H+��+2c��H2CO3��+c��HCO3-��=c��OH-��+c��Cl-�� | |
| D�� | pH=11����Һ�У�c��Na+����c��Cl-����c��CO32-����c��HCO3-����c��H2CO3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��0.1mol/LNaHCO3 ��Һ���У�c��Na+����c��HCO3-��+c��CO32-��+c��OH-�� | |
| B�� | ��NaHSO4��Һ���У�c��Na+��=c��SO42-��=c��H+�� | |
| C�� | ��������ˮ�м���KOH����Һ�����ԣ�����Һ���У�c��K+��=2c��ClO-��+C��HClO�� | |
| D�� | �������ʵ���Ũ�ȵ�Na2SO3��Һ��NaHSO4��Һ�������Ϻ�Ļ����Һ�У�c��OH-��-c��H2SO3��=c��H+��+c��SO32-�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com