
【题目】下列离子方程式正确的是( )
A.少量金属钠加到冷水中:Na+2H2O═Na++2OH﹣+H2↑
B.NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH﹣+HCO ![]() ═CaCO3↓+H2O
═CaCO3↓+H2O
C.硫酸铝溶液中加入过量氨水:Al3++4NH3?H2O═AlO ![]() +4NH
+4NH ![]() +2H2O
+2H2O
D.将2 mol/L? AlCl3溶液和7 mol/L? NaOH溶液等体积混合:2Al3++7OH﹣═Al(OH)3↓+AlO ![]() +2H2O
+2H2O
【答案】D
【解析】解:A.电子不守恒,正确的离子方程式为:2Na+2H2O═2Na++2OH﹣+H2↑,故A错误;B.酸式盐与碱发生反应时应该以不足量的物质Ca(OH)2为标准,正确的离子方程式是:Ca2++2OH﹣+2HCO ![]() ═CaCO3↓+H2O+CO
═CaCO3↓+H2O+CO ![]() ,故B错误;
,故B错误;
C.Al(OH)3只能被强酸、强碱溶解,正确的离子方程式是:Al3++3NH3H2O═Al(OH)3↓+3NH ![]() ,故C错误;
,故C错误;
D.假设溶液体积为1L,1L 2mol/LAlCl3溶液中含有2mol氯化铝,1L 7 mol/LNaOH溶液中含有7molNaOH,2mol铝离子完全反应生成氢氧化铝沉淀消耗6mol氢氧化钠,剩余的1mol氢氧化钠能够溶解1mol氢氧化铝,最终生成1mol氢氧化铝和1mol偏铝酸钠,反应的离子方程式为:2Al3++7OH﹣═Al(OH)3↓+AlO ![]() +2H2O,故D正确;
+2H2O,故D正确;
故选D.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】现有反应:mA(g)+nB(g)pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)m+np(填“>”“=”“<”).
(2)若加压时,A的质量分数 . (填“增大”“减小”或“不变”,下同)
(3)若加入A(体积不变),则B的转化率 .
(4)若降低温度,则平衡时B、C的浓度之比 ![]() 将 .
将 .
(5)若加入催化剂,平衡时气体混合物的总物质的量 .
(6)若B是有色物质,A、C均无色,维持容器内压强不变,充入氖气时,混合物颜色(填“变深”“变浅”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将11.2g铁粉和3.2g硫粉均匀混合,在密闭容器中加热到红热,冷却后加入足量的盐酸,在标准状况下收集到的气体体积为 ( )
A.11.2L B.5.6L C.4.48L D.2.24L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物分别是NaOH、NH3H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
①0.001mol/L的A溶液pH=3;
②B溶液和D溶液显碱性,等浓度两者PH关系B<D;
③E是弱电解质.回答下列问题:
(1)D是溶液,判断理由是 .
(2)用水稀释0.1molL﹣1 B时,溶液中随着水量的增加而减小的是(填写序号).
① ![]() ②
② ![]() ③c(H+)和c(OH﹣)的乘积 ④OH﹣的物质的量
③c(H+)和c(OH﹣)的乘积 ④OH﹣的物质的量
(3)将等体积、等物质的量浓度B和C的溶液混合,升高温度(溶质不会分解)溶液pH随温度变化为图中的曲线(填写序号).
(4)OH﹣浓度相同的等体积的两份溶液A和E,分别与锌粉反应,若最后仅有一份溶液中存在锌,放出氢气的质量相同,则下列说法正确的是(填写序号).
①反应所需要的时间E>A
②开始反应时的速率A>E
③参加反应的锌的物质的量A=E
④反应过程的平均速率E>A
⑤A溶液里有锌剩余
⑥E溶液里有锌剩余.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数的值,下列说法正确的是
A. 0.5 mol锌粒与足量盐酸反应产生11.2 L H2
B. 标准状况下,11.2 L CCl4所含分子数为0.5NA
C. 0.1 mol CH4所含氢原子数为0.4NA
D. 常温常压下,28 g N2中所含原子个数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
A.等体积、等物质的量浓度的明矾溶液和Ba(OH)2溶液混合:3Ba2++6OH﹣+2Al3++3SO ![]() ═2Al(OH)3↓+3BaSO4↓
═2Al(OH)3↓+3BaSO4↓
B.FeCl2在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH﹣
C.AlCl3(aq)中投入过量Na:2Al3++6Na+6H2O═2Al(OH)3↓+6Na++3H2↑
D.4molFeBr2(aq) 中通入3molCl2:2Fe2++4Br﹣+3Cl2═2Fe3++2 Br2+6Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,请计算出FeCl3、AlCl3的物质的量浓度各为多少? 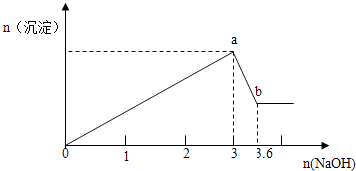
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.石油液化气的主要成份为甲烷
B.煤的干馏可分离出煤中含有的煤焦油
C.石油的分馏和食盐水的蒸馏原理上是相似的
D.石油经过分馏得到的汽油是纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com