

 .
. .
. .
.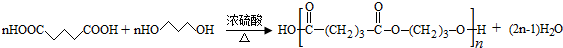 .
. (写结构简式):
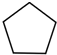
(写结构简式):分析 烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,其结构简式为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为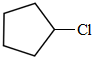 ,B发生消去反应生成C为
,B发生消去反应生成C为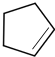 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG( ),以此来解答.
),以此来解答.
解答 解:烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢,$\frac{70}{12}$=5…10,则A为C5H10,结构简式为 ;A发生光照下取代反应生成B为
;A发生光照下取代反应生成B为 ,B发生消去反应生成C为
,B发生消去反应生成C为 ,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG(
,化合物C的分子式为C5H8;C发生氧化反应生成D为HOOC(CH2)3COOH,E、F为相对分子质量差14的同系物,F是福尔马林的溶质,则F为HCHO,可知E为CH3CHO,由信息④可知E与F反应生成G为OHCH2CH2CHO,G与氢气发生加成反应生成H为OHCH2CH2CH2OH,D与H发生缩聚反应生成PPG( ),
),
(1)根据分析可知,A的结构简式为: ,
,
故答案为: ;
;
(2)B为 、C为
、C为 ,由B生成C的化学方程式为:
,由B生成C的化学方程式为: ,
,
故答案为: ;
;
(3)由E和F生成G的反应类型为加成反应,G的结构简式为:OHCH2CH2CHO,
故答案为:加成反应;OHCH2CH2CHO;
(4)①由D和H生成PPG的化学方程式为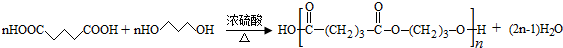 ,
,
故答案为: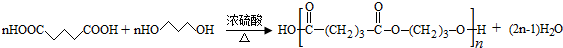 ;
;
②若PPG平均相对分子质量为10000,则其平均聚合度约为:$\frac{10000}{12×8+16×4+1×12}$≈58,
故答案为:a;
(5)D的同分异构体中能同时满足①能与饱和NaHCO3溶液反应产生气体,含-COOH,②既能发生银镜反应,又能发生皂化反应,则含有酯基-COOCH,D中共5个C,则含3个C-C-C上的2个H被-COOH、-OOCH取代,共为3+2=5种,含其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是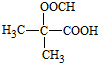 ,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,
,D及同分异构体中组成相同,由元素分析仪显示的信号(或数据)完全相同,
故答案为:5; ;c.
;c.
点评 本题考查有机物的推断,为高频考点,把握合成中碳链变化、官能团变化及反应条件推断物质为解答的关键,侧重分析与推断能力的综合考查,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 烃分子中,碳原子间都以碳碳单键结合,其余的价键均与氢原子结合,这一系列化合物的分子通式为CnH2n+2 | |
| B. | 分子组成相差一个或若干个CH2原子团的物质,互称为同系物 | |
| C. | 烷烃分子中,相邻的三个碳原子有可能在同一条直线上 | |
| D. | (CH3)2CH CH2CH2CH3、CH4、CH3CH2CH3互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “可燃冰”释放的甲烷属于烃 | |
| B. | “可燃冰”的分解与释放,可能会诱发海底地质灾害,加重温室效应 | |
| C. | “可燃冰”将成为人类的后续能源 | |
| D. | “可燃冰”是水变的油 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸的电离方程式:H2SO3?2H++SO32- | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式: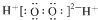 | |
| D. | 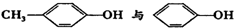 互为同系物 互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 (1)向含有等物质的量的SO32-、Fe2+、Br-、I-的溶液中,通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量关系如图所示.
(1)向含有等物质的量的SO32-、Fe2+、Br-、I-的溶液中,通入标准状况下的Cl2,通入Cl2的体积和溶液中相关离子的物质的量关系如图所示.| 阴离子 | SO42-、NO3-、Cl- |
| 阳离子 | Fe3+、Fe2+、NH4+、Cu2+、Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
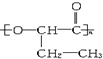 ,下列关于PHB的叙述中不正确的是( )
,下列关于PHB的叙述中不正确的是( )| A. | 它能发生水解反应 | |
| B. | 它在微生物作用下可降解成CO2和水 | |
| C. | 它可能是由一种含羟基的羧酸经缩聚反应而得 | |
| D. | 制备它的单体为HCOOH和CH3CH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
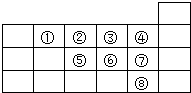 ①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示.
①~⑧是元素周期表中前四周期的8种元素,其相对位置如图所示. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
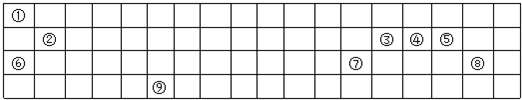
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com