
| 实验现象 | 结论 | |
| ① | 通电后,铁棒和石墨棒上都有气泡冒出 | |
| ② | 将阴极上方收集的气体靠近火焰,有爆鸣声 | |
| ③ | 阳极收集到的气体呈黄绿色,可使湿润的淀粉KI试纸变蓝 | |
| ④ | 铁棒一端的溶液滴加酚酞后变红 |
分析 通电后,铁棒和石墨棒上都有气泡冒出,说明两极都产生气体,将阴极上方收集的气体靠近火焰,有爆鸣声,说明生成氢气,阳极收集到的气体呈黄绿色,可使湿润的淀粉KI试纸变蓝,说明生成氯气,铁棒一端的溶液滴加酚酞后变红,说明阴极还有氢氧根产生,据此书写.
解答 解:通电后,铁棒和石墨棒上都有气泡冒出,说明两极都产生气体,将阴极上方收集的气体靠近火焰,有爆鸣声,说明生成氢气,阳极收集到的气体呈黄绿色,可使湿润的淀粉KI试纸变蓝,说明生成氯气,铁棒一端的溶液滴加酚酞后变红,说明阴极还有氢氧根产生,则电解饱和食盐水的化学方程式为:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑,故答案为:①两极都产生气体;②说明生成氢气;③说明生成氯气;④阴极还有氢氧根产生;2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+Cl2↑+H2↑.
点评 本题考查学生电解饱和食盐水产物的实验探究,难度不大,根据现象判断产物.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
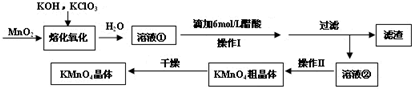
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入少量的KCl固体 | B. | 加入少量FeCl3固体 | ||
| C. | 降低Fe(SCN)3的浓度 | D. | 加水稀释 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
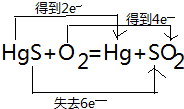 ,氧化剂是HgS、O2,还原产物:Hg、SO2.
,氧化剂是HgS、O2,还原产物:Hg、SO2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该金刚石粉末与水混和后能产生丁达尔现象 | |
| B. | 该反应属于置换反应 | |
| C. | CCl4和CH4在常温下均为无色气体 | |
| D. | 金刚石属于非金属单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加压 | B. | 减压 | C. | 升温 | D. | 减少E的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
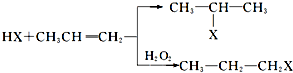 工业上按下列路线合成结构见识为:
工业上按下列路线合成结构见识为: 的物质,该物质的一种香料.
的物质,该物质的一种香料.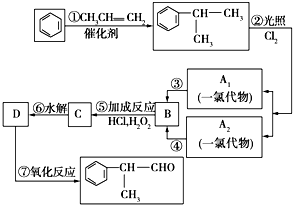
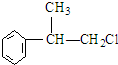 ;A2
;A2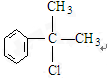 .
.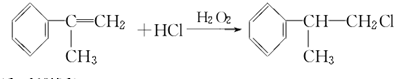 .
.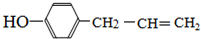 、,
、,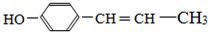 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35Cl和37Cl互为同位素 | |
| B. | 元素的化学性质主要取决于核外电子数 | |
| C. | 物质之间发生化学变化时,化学键一定发生变化 | |
| D. | 熔融状态下能够导电的化合物一定是离子化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com