
下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | Si有导电性 | Si可用于制备光导纤维 |
B | Fe的金属活动性大于Cu | FeCl3溶液可用于回收废旧电路板中的铜 |
C | Na2O2与水反应能生成碱 | Na2O2属于碱性氧化物 |
D | 次氯酸光照易分解 | 新制氯水保存在棕色试剂瓶中,放于冷暗处 |
A. A B. B C. C D. D
 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源:2017届辽宁省庄河市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
用下图所示实验装置进行实验研究(图中a、b、c表示止水夹),请对其方案进行完善或评价。
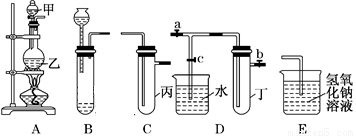
(1)实验室用装置A来制取Cl2,反应的离子方程式是______________;若将装置B、C、E相连后,用浓盐酸和______(填下列试剂的标号)为原料可制取Cl2。
a.KMnO4固体 b.KClO3固体 c.KCl固体 d.浓硫酸
(2)用装置B来制取制取氯气,并将装置B、C、E相连,在丙中加入适量水,即可制得氯水。向该氯水中加入大理石,充分振荡,观察到氯水的黄绿色逐渐褪去,同时产生少量气泡。某同学根据此现象推断出氯水呈酸性,请问该同学的推断是否合理?______________(填“合理”或“不合理”),若不合理,请说明理由(若合理,此空无需填写):_________________。
(3)为了探究氯水与大理石的反应,用装置A来制取氯气,并依次连接装置A、C、C、E。在第一个装置C的丙中,应加入的试剂是____________;在第二个装置C的丙中,加入适量水,即制得氯水。向制得的氯水中加入过量的大理石,反应结束后将所得溶液分成四等分,进行I、Ⅱ、Ⅲ、Ⅳ四个实验,实验操作如下,将实验现象或者实验结论填入下表:
实验序号 | 实验操作 | 实验现象 | 实验结论 |
Ⅰ | 将该溶液滴在有色布条上 | 有色布条迅速褪色 | ①该溶液中含有__________ |
Ⅱ | 向该溶液中滴加碳酸钠溶液 | ②___________ | 该溶液中含有Ca2+ |
Ⅲ | 向该溶液中滴加稀盐酸 | 有无色气泡产生 | ③无色气体是____________ |
Ⅳ | 加热该溶液 | 溶液变浑浊并产生大量气体 | ④该溶液中含有__________ |
⑤通过上述实验,得出氯水和过量的大理石反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:实验题
锰的化合物种类较多,大多具有广泛的用途。
Ⅰ.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
该小组设计了如下4个方案以验证MnO2的氧化性,可行的是__________(填序号)。
把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
Na2SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL0.2mol/L NaOH溶液、1mL水、1mL0.1mol/L稀硫酸。现象记录如表所示:
试管编号 | 实验现象 |
A | 溶液不变色 |
B | 溶液缓慢变浅棕褐色 |
C | 溶液迅速变棕褐色 |
①从以上实验中,我们可以得出的结论是_____________________。
②写出C试管中发生反应的离子方程式:_______________________。
Ⅱ.铁酸锰(MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如图:
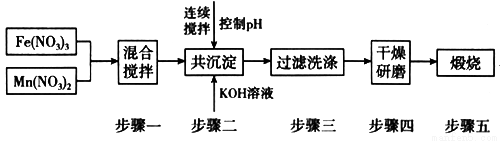
已知:Fe3+、Mn2+沉淀的pH如表格所示。
开始沉淀 | 完全沉淀 | |
Fe3+ | 2.7 | 4.2 |
Mn2+ | 8.3 | 10.4 |
步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为_________________。
步骤二中需控制pH的范围是_________________。
步骤三中是否洗涤干净的判断方法是_____________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省景德镇市高二(素质班)上学期期末考试化学试卷(解析版) 题型:选择题
下列物质与其用途完全符合的有几项( )
①SiO2——太阳能电池 ②NH3——制硝酸 ③NaCl——制纯碱 ④Al2O3——焊接钢轨
⑤NaClO——消毒剂 ⑥MgO——耐火材料 ⑦H2SO4——制炸药 ⑧Na2CO3——制水泥
A. 4 B. 5 C. 6 D. 7
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知乙溶液为无色溶液,则甲溶液中大量存在的离子是( )
A. Cu2+、H+、Cl- B. K+、OH- 、CO32- C. CO32-、OH-、Cl- D. K+、H+、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列化合物中,可以通过置换反应一步得到的是( )
①FeSO4 ②NaOH ③Fe3O4 ④Al2O3
A. ①②③④ B. ①②③ C. ①④ D. ①③
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省庄河市高一上学期期末考试化学试卷(解析版) 题型:选择题
N2和O2在一定条件下发生化合反应生成气体B,反应掉O2体积是反应掉N2的体积的1.5倍(同温同压),则B分子的组成是( )
A. N2O B. N2O3 C. NO2 D. N2O4
查看答案和解析>>
科目:高中化学 来源:2017届山东省淄博市高三第一次模拟考试化学试卷(解析版) 题型:实验题
锰酸锂(LiMn2O4)可作为锂离子电池的正极材料。工业上利用软锰矿浆吸收含硫烟气(SO2 和O2)制备锰酸锂,生产流程如下:
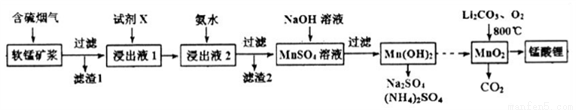
已知:①软锰矿主要成分为MnO2,含少量Fe2O3、FeO、Al2O3、SiO2等杂质。
②软锰矿浆在吸收含硫烟气的过程中酸性逐渐增强。
③部分氢氧化物沉淀相关的溶液pH如下表:
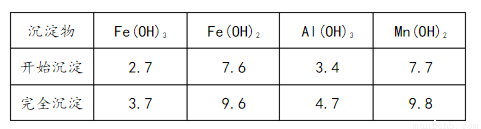
(1)已知:
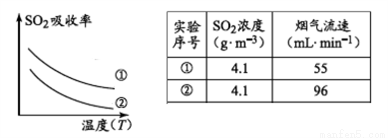
下列措施可提高SO2吸收率的是__________(填序号)
a.降低通入含硫烟气的温度 b.升高通入含硫烟气的温度
c.减少软锰矿浆的进入量 d.减小通入含硫烟气的流速
(2)加入试剂X能提高产品纯度,则X可以是_____________(填化学式)
(3)加氨水调溶液pH在5~6之间,目的是_______________。
(4)锰酸锂可充电电池的总反应式为:Li1-xMnO2+LixC  LiMn2O4+C(x<1)
LiMn2O4+C(x<1)
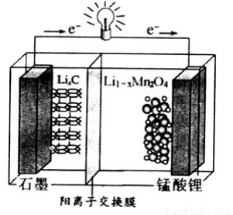
①放电时,电池的正极反应式为__________________
②充电时,若转移1mole-,则石墨电极将增重__________g。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省黄冈市高三第三次联考理综化学试卷(解析版) 题型:选择题
X、Y、Z、W、R为原子序数依次增大的五种短周期主族元素。X原子的最外层电子数是其内层电子数的2倍,W+与Y2-具有相同的电子层结构,R与Y可形成RY2、RY3化合物。下列说法正确的是
A. Y与氢元素所形成的化合物分子只含有极性键
B. W2Y、W2Y2中阴、阳离子个数比均为1:2
C. Z的最高价氧化物对应水化物的酸性比R的强
D. 将XY2通入W单质与水反应后的溶液中,生成的盐只有一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com