
| A. | 蛋白质 | B. | 天然气 | C. | 聚乙烯 | D. | 葡萄糖 |
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:解答题
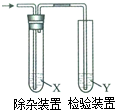 某同学在实验室完成以下实验:
某同学在实验室完成以下实验:查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | C | |
| B | D |
| A. | 气态氢化物的稳定性:HC>HD | |
| B. | 最高价氧化物对应水化物的酸性:H2BO4>HDO4 | |
| C. | 单质沸点最高的是B元素形成的单质 | |
| D. | A简单气态氢化物水溶液显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁锈的主要成分是Fe(OH)3 | |
| B. | 铁锈蚀过程中只发生了氧化还原反应 | |
| C. | 铁锈蚀与环境湿度和铁件密封程度有关 | |
| D. | 铁件发生电化学腐蚀时的负极反应式为Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和NaCl溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均变性了 |
| B | 将淀粉溶液和稀H2SO4混合加热后,再滴加新制的Cu(OH)2悬浊液,煮沸 | 无砖红色沉淀产生 | 淀粉未水解 |
| C | 向苯酚浓溶液中滴加少量溴水,振荡 | 无白色沉淀 | 苯酚与溴水不反应 |
| D | CH3COOH、C2H5OH和浓H2SO4共热制备CH3COOC2H5,将共热后产生的气体导入盛有饱和Na2CO3溶液的试管中 | 有油状物浮于Na2CO3溶液表面,振荡后,油状层变薄 | 证明油状物不全部是CH3COOC2H5 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com