
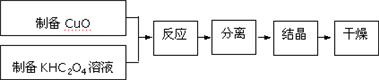
分析 (1)①根据过滤装置所需的玻璃仪器答题;
②CuO表面会附着硫酸根离子,用氯化钡溶液检验最后一次洗涤液中是否含有硫酸根离子判断是否洗涤干净;
(2)①过滤时滤纸上沾有大量的氧化铜固体,所以应直接将洗涤干净的氧化铜固体连同滤纸一起加入到草酸氢钾溶液中,充分反应后取出滤纸或将滤纸灼烧成灰再将剩余的固体转入热的KHC2O4溶液;
②CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O;
(3)由于草酸的酸性强于碳酸,所以可以用K2CO3粉末与草酸溶液反应制备KHC2O4;
(4)从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,可用加入少量乙醇,并用蒸馏的方法分离乙醇.
解答 解:(1)①过滤装置所需的玻璃仪器有漏斗、烧杯、玻璃棒,故答案为:漏斗、烧杯、玻璃棒;
②CuO表面会附着硫酸根离子,检验是否洗涤干净的具体方法是:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净,
故答案为:取最后一次洗涤滤液,滴入BaCl2溶液,若无白色沉淀,说明已洗涤干净;
(2)①过滤时滤纸上沾有大量的氧化铜固体,所以应直接将洗涤干净的氧化铜固体连同滤纸一起加入到草酸氢钾溶液中,充分反应后取出滤纸或将滤纸灼烧成灰再将剩余的固体转入热的KHC2O4溶液,故选ad;
②根据题意可知,CuO与KHC2O4溶液在50℃水浴加热条件下反应生成K2[Cu(C2O4)2]与H2O,反应的方程式为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O,
故答案为:2KHC2O4+CuO$\frac{\underline{\;50℃\;}}{\;}$K2[Cu(C2O4)2]+H2O;
(3)由于草酸的酸性强于碳酸,所以可以用K2CO3粉末与草酸溶液反应制备KHC2O4,故答案为:草酸的酸性强于碳酸;
(4)①从硫酸铜溶液中获得硫酸铜晶体时,为减少硫酸铜的溶解,降低硫酸铜的溶解度,有利于硫酸铜晶体析出,可用加入少量乙醇,
故答案为:降低硫酸铜的溶解度,有利于硫酸铜晶体析出;
②在蒸发浓缩的初始阶段还采用了蒸馏的方法,可起到回收乙醇的作用,故答案为:回收乙醇.
点评 本题考查物质的制备,为高频考点,侧重于学生的分析能力和实验能力的考查,注意把握物质的性质以及实验的原理和操作,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届江西省高三上学期期中化学试卷(解析版) 题型:选择题
下列指定反应的离子方程式正确的是
A.氨水溶解氯化银沉淀:AgCl+2NH3·H2O=[Ag(NH3)2]++ Cl-+2H2O
B.向Na2S2O3溶液中通入足量氯水:S2O32-+ 2Cl2 +3H2O==2SO32-+4Cl-+6H+
C.酸性K2Cr2O7溶液氧化双氧水:Cr2O72-+8H++5H2O2=2Cr3++4O2↑+9H2O
D.1.0mol/L的NaAlO2溶液和2.54mol/L盐酸等体积混合:AlO2-+4H+=5Al3++2H2O
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上期中化学试卷(解析版) 题型:选择题
将下列物质按酸、碱、盐分类依次排列正确的是
A.硫酸、纯碱、石灰石 B.氢硫酸、烧碱、绿矾
C.石炭酸、熟石膏、醋酸钠 D.磷酸、乙醇钠、苛性钾
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.
硫酸亚铁铵是一种浅蓝绿色晶体,俗称摩尔盐.| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 70 |
| (NH4)2SO4 | 73.0 | 75.4 | 78.0 | 81.0 | 84.5 | 91.9 |
| FeSO4•7H2O | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| 摩尔盐 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com