(2010?朝阳区一模)工业上以氨气为原料制备硝酸的过程如图1所示:
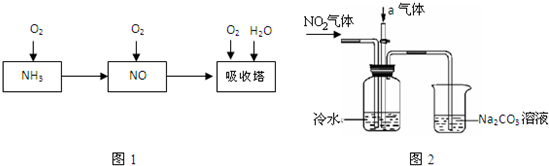
某课外小组模拟上述部分过程设计了如图2所示实验装置制备硝酸(所有橡胶制品均已被保护).
(1)工业上用氨气制取NO的化学方程式是
.
(2)连接好装置后,首先进行的操作是
检验装置的气密性
检验装置的气密性
.
(3)通入a气体的目的是
提高NO2的转化率
提高NO2的转化率
.
(4)盛有Na
2CO
3溶液的烧杯为尾气处理装置,该装置中发生反应的化学方程式是2NO
2+Na
2CO
3═NaNO
2+
NaNO3
NaNO3
+
CO2
CO2
(5)已知:温度低于21.15℃时,NO
2几乎全部转变为N
2O
2.工业上可用N
2O
4与水反应来提高硝酸产率.N
2O
4与a气体在冷水中生成硝酸的化学方程式是
2N2O4+O2+2H2O=4HNO3
2N2O4+O2+2H2O=4HNO3
.
(6)一定条件下,某密闭容器中N
2O
4和NO
2的混合气体达到平衡时,c(NO
2)=0.500mol/L,c(N
2O
4)=0.125mol/L.则2NO
2(g)?N
2O
4(g)的平衡常数K=
.若NO
2起始浓度为2mol/L,相同条件下,NO
2的最大转化率为
50%
50%
.




 科学实验活动册系列答案
科学实验活动册系列答案