
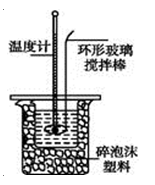
【题目】用100mL 1.00mol·L-1盐酸与100mL 1.10mol·L-1NaOH溶液在如下图所示的装置中进行中和热测定实验。以下是四次实验所得数据。回答下列问题:
实验 数据 | 盐酸起始温度t1/℃ | 氢氧化钠起始温度t2/℃ | 两溶液混合后 温度t3/℃ |
1 | 21.0 | 21.1 | 26.9 |
2 | 21.5 | 21.7 | 28.2 |
3 | 21.9 | 22.1 | 28.7 |
4 | 22.3 | 22.5 | 29.2 |
(1)上表中的温度差平均值为 ℃
(2)近似认为上述两种溶液的密度都是1 g·cm-3,中和后生成溶液的比热容c=4.18J·(g·℃)-1。则计算得到中和热ΔH= (取小数点后一位)。
(3)上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母) 。
a.实验装置保温、隔热效果差
b.用环形铜质搅拌棒代替环形玻璃搅拌棒
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定盐酸溶液起始温度后直接测定NaOH溶液的温度
【答案】(1)6.7;(2)-56.0kJ/mol;(3)a、b、c、d。
【解析】
试题分析:(1)第一组数值与其他数值相差较大,因此第一组数值忽略不计,第2组中盐酸和氢氧化钠平均温度为21.6℃,两溶液混合后的温度与混合前的温度差为(28.2-21.6) =6.6℃,第三组混合前的平均温度是22.0℃,混合后和混合前的温差是6.7℃,第四组混合前的平均温度为22.4℃,混合后的温度和混合前的温度差为(29.2-22.4)=6.8℃,因此平均温度差为6.7℃;(2)根据△H=-cm△t/n(H2O)=-4.18×10-3×200×6.7/(100 × 10-3 × 1) kJ·mol-1 = -56.0 kJ·mol-1;(3)a、根据(2)计算出的中和热小于57.3,造成热量的损失,实验装置保温、隔热效果差,造成热量损失,热量减小,故正确;b、铜导热效果好,造成热量的损失,故正确;c、多次把NaOH溶液倒入盛有盐酸的小烧杯中,造成热量损失,故正确;d、发生中和反应,造成温度升高,温差减小,故正确。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】下表是A、B、C、D、E五种有机物的有关信息:
A | B | C | D | E |
①是一种烃,能使溴的四氯化碳溶液褪色 ②比例模型为:
③能与水在一定条件下反应生成C | ①由C、H两种元素组成 ②球棍模型为:
| ①能与钠反应,但不能与NaOH溶液反应; ②能与E反应生成相对分子质量为100的酯 | ①由C、H、Br三种元素组成; ②相对分子质量为109 | ①由C、H、O三种元素组成; ②球棍模型为:
|
根据表中信息回答下列问题:
(1)写出A使溴的四氯化碳溶液褪色的化学方程式:__________________;
(2)A与氢气发生加成反应后生成分子F,F的同系物的通式为CnH2n+2。当n =________时,这类有机物开始有同分异构体。
(3)B的分子式为____________,写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:___ ;
(4)C与E反应能生成相对分子质量为100的酯,写出该反应的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是
A.Fe -2e-=Fe2+ B.2H2O+O2+4e-=4OH-
C.2H++2e-=H2↑ D.4OH-- 4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是( )
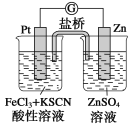
A.该原电池的正极反应是Zn-2e-=Zn2+
B.左侧烧杯中溶液的血红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为3Zn+2Fe3+=2Fe+3Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于50mL密度为1.40gmL﹣1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体 1 120mL(标准状况),向反应后的溶液中加入1.0molL﹣1NaOH溶液,当金属离子全部沉淀时,得到2.54g沉淀.下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是1:2
B.该浓硝酸中HNO3的物质的量浓度是14.0 molL﹣1
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54 g沉淀时,加入NaOH溶液的体积是640 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将如图所示实验装置的K闭合,下列判断正确的是( )
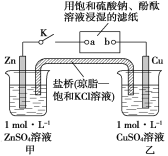
A.电子沿Zn→a→b→Cu路径流动
B.Cu电极上发生还原反应
C.片刻后甲池中c(SO![]() )增大
)增大
D.片刻后可观察到滤纸b点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤。在无机非金属材料中,硅一直扮演着主角。下面几种物质中含有硅单质的是( )
A.太阳能电池板 B.水晶 C.玛瑙 D.光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(气)![]() bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的60%,则
bB(气)达到平衡后,保持温度不变,将容器体积增大一倍,当达到新平衡时,B的浓度是原来的60%,则
A. 平衡向逆反应方向移动了 B. 物质A的转化率减小了
C. 物质B的质量分数增加了 D. a>b
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com