
在一定条件下可实现如图所示物质之间的变化:
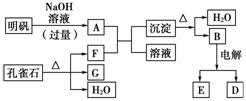
请填写下列空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,上图中的F是________。
(2)写出明矾与过量NaOH溶液反应的离子方程式:
________________________________________________________________________
________________________________________________________________________。
(3)图中所得G和D都是固体,混合后在高温下可发生反应,写出该反应的化学方程式:____________________________。
(4)每生成1 mol D,同时生成________mol E。
解析: A是Na[Al(OH)4],有关反应为Al3++4OH-===[Al(OH)4]-,孔雀石受热分解的方程式为CuCO3·Cu(OH)2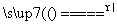 2CuO+CO2↑+H2O,则F应是CO2,G是CuO;A与F反应的方程式为CO2+[Al(OH)4]-===Al(OH)3↓+HCO
2CuO+CO2↑+H2O,则F应是CO2,G是CuO;A与F反应的方程式为CO2+[Al(OH)4]-===Al(OH)3↓+HCO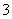 (或CO2+2[Al(OH)4]-===2Al(OH3)↓+CO
(或CO2+2[Al(OH)4]-===2Al(OH3)↓+CO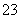 +H2O),沉淀是Al(OH)3,受热分解得到H2O和Al2O3(B);Al2O3电解生成Al和O2。因D为固体,则D是Al,E是O2;Al和CuO的反应类似于铝热反应;最后一问可用反应式2Al2O3
+H2O),沉淀是Al(OH)3,受热分解得到H2O和Al2O3(B);Al2O3电解生成Al和O2。因D为固体,则D是Al,E是O2;Al和CuO的反应类似于铝热反应;最后一问可用反应式2Al2O3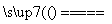 4Al+3O2↑来计算。
4Al+3O2↑来计算。
答案: (1)CO2 (2)Al3++4OH-===[Al(OH)4]-
(3)3CuO+2Al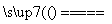 Al2O3+3Cu (4)
Al2O3+3Cu (4)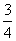


科目:高中化学 来源: 题型:
已知某溶液中存在较多的H+、SO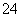 、NO
、NO ,则该溶液中还可能大量存在的离子组是( )
,则该溶液中还可能大量存在的离子组是( )
A.Al3+、CH3COO-、Cl- B.Mg2+、Ba2+、Br-
C.Mg2+、Cl-、I- D.Na+、NH 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)CO2的相对分子质量为______________,它的摩尔质量为________。
(2)在标准状况下,0.5 mol任何气体的体积都约为________。
(3)4 g H2与22.4 L(标准状况)CO2相比,所含分子数目较多的是________。
(4)0.01 mol某气体的质量为0.28 g,该气体的摩尔质量为__________,在标准状况下,该气体的体积是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于实验现象的解释不正确的是( )
A.铝在空气中能很快形成氧化膜 B.氧化铝薄膜兜住了熔化的铝
C.氧化铝的熔点比铝高 D.铝箔表面温度低,未熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物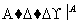 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物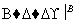 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是( )
A.溶液A和B均可以是盐酸和NaOH溶液
B.溶液A和B均可以选用稀硝酸
C.若溶液B选用浓硝酸,则测得铜的质量分数偏小
D.实验方案Ⅱ更便于实施
查看答案和解析>>
科目:高中化学 来源: 题型:
要使相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中所含SO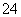 的数目相同,则所取两溶液的体积比是( )
的数目相同,则所取两溶液的体积比是( )
A.1∶3 B.3∶1
C.3∶2 D.2∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是( )
A.从1 L 1 mol·L-1的NaCl溶液中取出10 mL,其浓度仍是 1 mol·L-1
B.制成0.5 L 10 mol·L-1的盐酸,需要HCl气体112 L(标准状况)
C.0.5 L 2 mol·L-1的BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023
D.10 g 98%的硫酸(密度为1.84 g·cm-3)与10 mL 18.4 mol·L-1的硫酸的浓度是不同的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com