
元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如右图所示。
①在1个晶胞中,X离子的数目为______。
②该化合物的化学式为__________。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_____。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是____________________。
(4)Y 与Z 可形成YZ42-,则: YZ42-的空间构型为________________(用文字描述)。
写出一种与YZ42-互为等电子体(价电子数相同)的分子的化学式:______________。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为_________。
科目:高中化学 来源:2016-2017学年湖北省高二2月联考化学试卷(解析版) 题型:选择题
下列各离子组在指定的溶液中一定能大量共存的是
①常温在c(H+)/c(OH-)=10-10溶液中:K+、Na+、CH3COO-、SO42﹣
②常温pH=11的溶液中:CO32﹣、Na+、AlO2﹣、NO3﹣
③水电离出的H+浓度c(H+)=10﹣12mol•L?1的溶液中:Cl﹣、NO3﹣、Na+、S2O32﹣
④使甲基橙变红色的溶液中:Fe3+、NO3﹣、Na+、SO42﹣
A.①②③ B.①②④ C.②③④ D.①③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期第一次月考化学试卷(解析版) 题型:填空题
用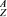 X表示原子:
X表示原子:
(1)中性原子的中子数:N=________。
(2)阳离子的中子数:AXn+共有x个电子,则N=________。
(3)阴离子的中子数:AXn-共有x个电子,则N=________。
(4)中性分子中子数:12C18O2分子中,N=________。
(5)A2-原子核内有x个中子,其质量数为m,则n gA2-所含电子的物质的量为________mol。
(6)某元素的同位素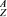 X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:
X,其氯化物XCl2。1.11 g溶于水制成溶液后,加入1 mol/L的AgNO3溶液20 mL恰好完全反应。若这种同位素原子核内有20个中子,则:
①Z值和A值:Z=________,A=________;
②X元素在周期表中的位置_____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列过程中,共价键被破坏的是
A.碘升华 B.溴蒸气被木炭吸附
C.酒精溶于水 D.HCl气体溶于水
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法中,不正确的是
A. 双原子分子中的共价键,一定是非极性键
B. 非极性键也可能存在于离子化合物中
C. 分子间作用力比化学键要弱得多
D. 共价化合物在液态时不能导电
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷(解析版) 题型:填空题
下表为元素周期表前三周期的一部分。
X | Z | ||
W | Y | R | |
(1)X的氢化物的沸点与W的氢化物比较,沸点较高的是:______________(填化学式),原因是_____________________。
(2)从下列选项中选出X的基态原子的最外层原子轨道表示式____________,另一原子轨道表示式不能作为基态原子的轨道表示式是因为它不符合____________。(填序号)。
A. 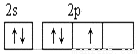 B.
B. 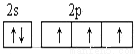
C.泡利原理 D.洪特规则
(3)以上W、Y、R元素原子失去核外第一个电子需要能量由多到少的顺序为:_______________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷(解析版) 题型:选择题
下列说法中正确的是( )
A. 第3周期所含元素中钠的第一电离能最小
B. 铝的第一电离能比镁的第一电离能大
C. 在所有的元素中,F的第一电离能最大
D. 钾的第一电离能比镁的第一电离能大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都简阳市高一上学期期末检测化学试卷(解析版) 题型:实验题
为了探究木炭与浓H2SO4反应的产物中是否存在CO2,某同学选用如图所示装置进行实验:
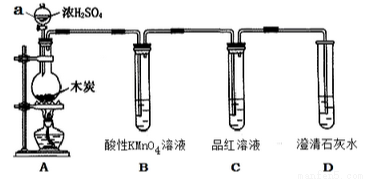
(1)仪器a的名称为:__________;在组装好上述实验装置后,在装入药品之前必需的实验操作是________________。
(2)写出A中发生反应的化学方程式____________________。该装置还可以用于实验室制取Cl2,请写出实验室制取Cl2的离子方程式并用单线桥标明电子转移________________。
(3)装置B的作用是____________________。
(4)能说明产物中一定存在CO2气体的实验现象为________________。
(5)质量分数为98%的浓硫酸,其密度为1.84g/ml,该浓硫酸的物质的量浓度为__________,用该硫酸配制500ml 0.5mol/L的稀硫酸,主要仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要____________,定容时由于俯视刻度线,则对浓度产生的影响为___________ (填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市高二3月学生学业能力调研化学试卷(解析版) 题型:选择题
最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”—全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划。有关全氟丙烷的说法正确的是 ( )
A.分子中三个碳原子可能处于同一直线上
B.全氟丙烷的电子式为: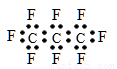
C.相同压强下,沸点:C3F8<C3H8
D.全氟丙烷分子中既有极性键又有非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com