

���� ��1�������Ȼ�ѧ����ʽ��˹���ɼ����+��õ�CO2��NH3�ϳ����غ���̬ˮ���Ȼ�ѧ��Ӧ����ʽ����H-T��S��0�ķ�Ӧ�ܹ��Է����У�
��2��A��CO2��NH3Ϊԭ�Ϻϳ����صķ�Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У���С������Ũ��ƽ�������ƶ����������ǹ��壬�ݴ˷�����
B���¶ȵ���190��ʱ��Ӧû�дﵽƽ��״̬��
C�����¶���190��ʱ��Ӧ�ﵽƽ��״̬���¶����{ƽ�������ƶ���
D����ͼ������ˮ̼��Խ�������̼ת����Խ�ͣ�
��3�������Ȼ�ѧ����ʽ2NH3��g��+CO2��g��?NH2CO2NH4��s�����ƽ�ⳣ���ĸ����ͼ�����ݼ������淴Ӧ��ƽ�ⳣ����ͼ�����������̼��ƽ��Ũ��Ϊ0.025mol/L�������Сһ��Ũ������һ��ӦΪ0.05mol/L���淴Ӧ���дﵽƽ��״̬����Ϊ������Ϊ���壬���ﵽ��ͬƽ��״̬��������̼Ũ�Ȳ��䣬�ݴ˻����仯���ߣ�
��4������[CO��NH2��2]�еĵ���-3�۵�0�ۣ�����������Ӧ��AΪ�������ݴ˷�����
��� �⣺��1����2NH3��g��+CO2��g��=NH2CO2NH4��s����H=-l59.47kJ•mol-1
��NH2CO2NH4��s��=CO��NH2��2��s��+H2O��g����H=+72.49kJ•mol-1
�����Ȼ�ѧ����ʽ��˹���ɼ����+��õ�CO2��NH3�ϳ����غ���̬ˮ���Ȼ�ѧ��Ӧ����ʽΪ2NH3��g��+CO2��g��?CO��NH2��2��s��+H2O��g����H=-86.98kJ•mol-1����Ӧ II��NH2COONH4��s��?CO��NH2��2��s��+H2O��g����H2=+72.49KJ•mol-1Ϊ���������������ȷ�Ӧ����ʹ��H-T��S��0����������£�
�ʴ�Ϊ��2NH3��g��+CO2��g��?CO��NH2��2��s��+H2O��g����H=-86.98kJ•mol-1�����£�
��2��A��CO2��NH3Ϊԭ�Ϻϳ����صķ�Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У�ƽ�ⳣ����С������Ϊ���壬���߲������ض�������Ũ��û��Ӱ�죬ƽ�ⲻ�ƶ�����A����
B���¶ȵ���190��ʱ��Ӧû�дﵽƽ��״̬�����Զ�����̼��ת����������B����
C�����¶���190��ʱ��Ӧ�ﵽƽ��״̬��CO2��NH3Ϊԭ�Ϻϳ����صķ�Ӧ�Ƿ��ȷ�Ӧ������ƽ��������У�������̼ת���ʼ�С����C����
D����ͼ������ˮ̼��Խ�������̼ת����Խ�ͣ���D����
�ʴ�Ϊ��ABCD��
��3����ͼ��֪ƽ��״̬ʱc��CO2��=0.025mol/L����Ӧ��0.075mol/L����ƽ��ʱc��NH3��=0.05mol/L����Ӧ��2NH3��g��+CO2��g��?NH2CO2NH4��s����H1=-159.47kJ•mol-1�����淴Ӧ��ƽ�ⳣ��K=[NH3]2��[CO2]=0.052��0.025=6.25��10-5����
�ں����½�0.4mol NH3��0.2mol CO2�����ݻ�Ϊ2L���ܱ������У��ﵽƽ��ʱ��
2NH3��g��+CO2��g��?NH2CO2NH4��s��
��ʼ����mol/L�� 0.2 0.1 0
�仯����mol/L�� 0.15 0.075
ƽ������mol/L�� 0.05 0.025
t1ʱ�ﵽƽ�������c��CO2����ʱ��t�仯����������ͼ2��ʾ���������������䣬t1ʱ���������ѹ����1L��������̼Ũ��Ӧ����0.05mol/L��ѹǿ����ƽ��������У������������ǹ��壬���Դﵽƽ��״̬��������̼Ũ�ȱ��ֲ��䣬�ݴ˻����仯����Ϊ��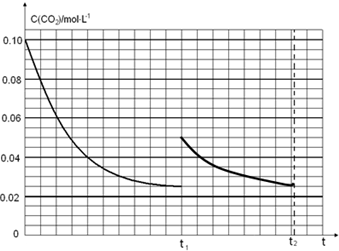 ��
��
�ʴ�Ϊ��6.25��10-5�� ��
��
��4������[CO��NH2��2]�еĵ���-3�۵�0�ۣ�����������Ӧ��AΪ�������缫��ӦʽΪ��CO��NH2��2-6e-+8OH-=CO32-+N2��+6H2O���ʴ�Ϊ��CO��NH2��2-6e-+8OH-=CO32-+N2��+6H2O��
���� ���⿼���˸�˹���ɵ�Ӧ�á���ѧƽ��״̬���������ƽ��ת���ʵ����㡢����ʽ����д�͵缫��Ӧʽ����д����Ŀ�Ѷ��еȣ��������ؼ�Ҫ����ͼ�����ĺ��壬����ƽ��������⣮


 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�� | B�� | ���� | C�� | ��ˮ�� | D�� | ǿ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HF��H2O��CH4��SiH4���ȶ���������ǿ | |
| B�� | �����뾶�Ӵ�С˳��K��Cl��K+ | |
| C�� | C��N��O��FԪ�ص���������ɵ͵��� | |
| D�� | ��ͬ�¶�ʱ���ʵ���Ũ����ȵ�NaCl��MgCl2��AlCl3������Һ��pHֵ��С���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʱ��/s | 0 | 500 | 1000 | 1500 |
| c��N2O5��/mol•L-1 | 5.00 | 2.25 | 2.50 | 2.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���һЩ�����ﳣ�����뵼�塢���ݼ���ɱ��ҩ�ȣ��ش��������⣺
���һЩ�����ﳣ�����뵼�塢���ݼ���ɱ��ҩ�ȣ��ش��������⣺
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ʵ���Ũ�ȵ�����������Һ��̼�������Һ��ϣ�Ba2++2OH-+NH4++HCO3-=BaCO3��+NH3•H2O+H2O | |
| B�� | ʵ�������Ƶ���������Һ�ڿ����б�������4Fe2++O2+2H2O=4Fe3++4OH- | |
| C�� | ��̼�������Һ�мӹ���ʯ��ˮ�����ȣ�NH4++OH-$\frac{\underline{\;��\;}}{\;}$NH3��+H2O | |
| D�� | ���ữ�ĸ��������Һ����˫��ˮ��2MnO4-+6H++H2O2�T2Mn2++3O2��+4H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���200mL 0.1mol•L-1CH3COONa��Һ�У�����0.1mol•L-1���ᣨ�����ǻӷ�����CH3COOH��CH3COO-���ʵ����������������ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
�����£���200mL 0.1mol•L-1CH3COONa��Һ�У�����0.1mol•L-1���ᣨ�����ǻӷ�����CH3COOH��CH3COO-���ʵ����������������ı仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ����������룬��Һ��ˮ�ĵ���̶������� | |
| B�� | ����������룬$\frac{c��O{H}^{-}��}{c��C{H}_{3}CO{O}^{-}��}$������ | |
| C�� | M �㣬n��H+��-n��OH-��=��a��10-4-0.01��mol | |
| D�� | �� V�����ᣩ=200mLʱ��c��CH3COO-��+c��CH3COOH����c��Cl-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
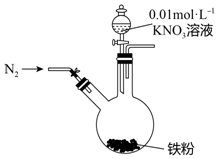 ijͬѧ�����������������ԭNO3-�ѳ�����ˮ�������Ρ���������Ϻ���������װ��̽��������KNO3��Һ�ķ�Ӧ��ʵ�鲽�輰�������£�
ijͬѧ�����������������ԭNO3-�ѳ�����ˮ�������Ρ���������Ϻ���������װ��̽��������KNO3��Һ�ķ�Ӧ��ʵ�鲽�輰�������£�| ʵ�鲽�� | ʵ������ |
| 1�����ɼУ�����ͨ��N2 | |
| 2������pHΪ2.5��0.01mol/L����KNO3��Һ100mL | ���۲����ܽ⣬��Һ��dz��ɫ�� ���۲����ܽ��ʣ�����۱������������ɫ���ʸ��ţ� |
| 3����Ӧֹͣ�ε���������Բ����ƿȡ�� | ��ƿ���������ɫû�з����仯�� |
| 4��ʣ�������� | ����İ�ɫ���ʱ�Ϊ���ɫ�� |
| ʵ�鲽�� | ʵ������ |
| 1��ȡ������Һ���Թ��У������м���KSCN��Һ | ��ҺҺ�ޱ仯 |
| 2����������Һ��Ϊ���ݣ�һ���е�����������һ���еμ�ϡ���� | ������Һ����Ϊ��ɫ |
| 3����ȡ������Һ���Թ��У������м���ŨNaOH��Һ�����ȣ����Թܿڷ���ʪ��ĺ�ɫʯ����ֽ�� | ���������ɣ�������ʹ��ɫʯ����ֽ������ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com