
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.1mol 羟基(—OH)中电子数为9NA
B.100 mL 2.0 mol·L -1的盐酸与醋酸溶液中氢离子数均为0.2NA
C.将10.6 g Na2CO3固体溶于水,所得离子总数为0.3NA
D.常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源:2015-2016学年辽宁东北育才学校高一下第二段考化学试卷(解析版) 题型:推断题
已知A是一种重要的基本化工原料,其分子中碳元素的百分含量为85.7%,且相对分子量小于30。A、B、C、D、E、F、G、H有下图所示的转化关系(部分产物已略去)。其中B为高分子化合物,C为无色无味气体,实验室中可以通过G与大理石制取。D为烃,不能使酸性高锰酸钾溶液褪色。E、G为生活中常见的有机物,且E有特殊香味,H有香味。
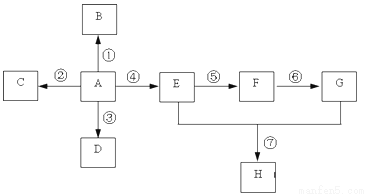
(1)写出下列各物质的官能团的名称:A ___________;E ___________;
(2)按要求写出下列各步变化的化学方程式(注明反应条件)
反应①_____________________________________________________;
反应④_____________________________________________________;
反应⑦ _____________________________________________________。
(3)写出下列反应类型:反应① ___________,反应②___________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁东北育才学校高二下第二段考化学试卷(解析版) 题型:选择题
下列实验的操作和所用的试剂都正确的是( )
A.要检验己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液
B.配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中
C.制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热
D.除去乙酸乙酯中少量的乙酸,可以加氢氧化钠溶液后分液
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨六中高三下三模理综化学试卷(解析版) 题型:选择题
化学与生产、生活密切相关。下列叙述中不正确的是
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.西非国家曾爆发埃博拉疫情,埃博拉病毒对化学药品敏感,乙醇、次氯酸钠溶液均可以将病毒氧化而达到消毒的目的
C.硅胶可用作食品干燥剂
D.燃料脱硫,脱氮都是减少酸雨的有效措施
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:填空题
碘化钠在医药中用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,也用作食品添加剂、感光剂等。 工业上用NaOH溶液、水合肼制取碘化钠固体,其制备流程图如下:

已知:N2H4·H2O在100℃以上分解。
(1)已知,在合成过程的反应产物中含有NaIO3,则在合成过程中消耗了3 mol I2,所生成 NaIO3的物质的量为 mol。
(2)写出还原过程中的离子方程式 ;在还原过程中,为了加快反应,可采取可提高反应温度,但温度不得超过 ℃;请选择下列试剂检测所得碘化钠固体中是否含有NaIO3杂质 (选填字母)。
A.FeCl2溶液 B.冰醋酸
C.KI溶液 D.淀粉溶液
(3)测定产品中NaI含量的实验步骤如下:
a.称取4.000g 样品、溶解,在250mL 容量瓶中定容;
b.量取25.00ml 待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入A溶液作指示剂;
c.用 0.1000mol·L -1 的Na2S2O3,溶液进行滴定至终点(发生反应的方程式为:
2Na2S2O3 +I2===Na2S4O2 +2NaI),重复测定2次,所得的相关数据如下表:
测定 序号 | 待测液体积/ mL | 标准液滴定管起点读数/ mL | 标准液滴定管终点读数/ mL |
1 | 25.00 | 0.06 | 24.04 |
2 | 25.00 | 0.02 | 24.02 |
3 | 25.00 | 0.12 | 24.14 |
①操作b中,加入足量的FeCl3溶液时所发生的离子方程式为 。
②加入A物质为 (填名称);滴定终点观察到的现象为 。
③计算该样品中NaI的含量为 。
(只写出有具体数值的表达式即可)
(4)碘化钠固体的保存方法是 。
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三考前高考模拟十化学试卷(解析版) 题型:选择题
同位素示踪法可用于反应机理的研究,下列反应或转化中同位素示踪表示正确的是
A.2Na218O2 +2H2O====4Nal8OH+O2↑
B.NH4Cl+ 2H2O====NH3·2H2O+HCl
C.2KMnO4 +5H218O2 +3H2SO4====K2SO4+2MnSO4 +518O2↑+8H2O
D.K37ClO3+6HCl===K37Cl+3Cl2↑+3H2O
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三临考模拟化学试卷(解析版) 题型:填空题
有一混合物水溶液,含有以下离子中的若干种:Na+、NH4+、Cl—、Ba2+、HCO3—、SO42—,现各取100mL溶液分别进行如下实验:
①第一份加入AgNO3溶液有沉淀产生
②第二份加足量NaOH溶液,加热,收集到标准状况下的气体448mL
③第三份加足量Ba(OH)2溶液,得沉淀4.30g,再用足量盐酸洗涤、干燥后,沉淀质量为2.33g。
根据上述实验,回答以下问题:
(1)由第一份进行的实验推断该混合物是否一定含有Cl-:____________;(填“是”或“否”)
(2)由第二份进行的实验可知混合物中应含有____________离子,其物质的量浓度为____________;
(3)由第三份进行的实验可知4.30g沉淀的成份为____________,写出生成该沉淀的离子方程式:____________;
(4)溶液中肯定存在的离子是____________。
查看答案和解析>>
科目:高中化学 来源:2016届海南省高三考前预测化学试卷(解析版) 题型:选择题
目前,世界上已经合成了几百种有机超导体,下图所示是其中之一,该分子结构如下图所示.下列关于该化合物说法错误的是( )

A.分子中所有的氮原子在同一平面内
B.属于芳香烃
C.分子式为C12H4N4
D.该物质易溶于水
查看答案和解析>>
科目:高中化学 来源:2016届贵州省高三5月高考模拟理综化学试卷(解析版) 题型:填空题
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才.现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)△H<0.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.
2NH3(g)△H<0.当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如图所示.

回答下列问题:
(1)已知:①NH3(l)═NH3(g)△H1,②N2(g)+3H2(g) 2NH3(l)△H2;则反应N2(g)+3H2(g)
2NH3(l)△H2;则反应N2(g)+3H2(g) 2NH3(g)的△H=_____________(用含△H1、△H2的代数式表示)。
2NH3(g)的△H=_____________(用含△H1、△H2的代数式表示)。
(2)合成氨的平衡常数表达式为____________,平衡时,M点NH3的体积分数为10%,则N2的转化率为____________(保留两位有效数字).
(3)X轴上a点的数值比b点____________(填“大”或“小”)。上图中,Y轴表示____________(填“温度”或“压强”),判断的理由是____________。
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如表所示:
容器编号 | 实验条件 | 平衡时反应中的能量变化 |
Ⅰ | 恒温恒容 | 放热Q1kJ |
Ⅱ | 恒温恒压 | 放热Q2kJ |
Ⅲ | 恒容绝热 | 放热Q3kJ |
下列判断正确的是____________
A.放出热量:Ql<Q2<△Hl
B.N2的转化率:Ⅰ>Ⅲ
C.平衡常数:Ⅱ>Ⅰ
D.达平衡时氨气的体积分数:Ⅰ>Ⅱ
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)____________c(SO42-)(填“>”、“<”或“=”).
(6)利用氨气设计一种环保燃料电池,一极通入氨气,另一极通入空气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-.写出负极的电极反应式____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com