
| A. | 平均相对分子质量 | B. | 密度 | ||
| C. | 容器内的压强 | D. | 物质的量 |
分析 升高温度,化学平衡向着吸热方向进行,所以化学平衡2M(g)?N(g)发生移动,混合物的物质的量发生变化,平均分子量也变化,但是气体的总质量是守恒的,所以质量不变,所以总的物质的量变化,所以压强会发生改变,气体的总质量是守恒的,烧瓶的体积也是不变的,所以密度不变,由此分析解答.
解答 解:A、反应两边都是气体,气体的总质量不变,反应方程式两边气体的体积不相等,升高温度,平衡发生移动,混合物的物质的量发生变化,平均分子量也变化,所以反应前后气体的平均分子量不相同,故A错误;
B、反应两边都是气体,气体的总质量不变,烧瓶的容积固定,根据$ρ=\frac{m}{V}$,气体的密度一定不会变化,故B正确;
C、由于升高温度,平衡发生移动,混合物的物质的量发生变化,所以压强也变化,故C错误;
D、方程式两边气体的体积不相等,升高温度,平衡发生移动,混合物的物质的量发生变化,所以反应前后气体的物质的量不相等,故D错误;
故选B.
点评 本题考查了温度对化学平衡的影响,题目难度中等,可以根据平衡移动原理判断温度对化学平衡的影响,试题侧重对学生灵活运用基础知识解决实际问题的能力的培养.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

| 化学键 | H-H | C-O | H-O | C-H |
| E/(kJ•mol-1) | 436 | 343 | 465 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硝基苯的结构简式: | |
| B. | 氮气的电子式: | |
| C. | 中子数为 146、质子数为92的铀(U)原子:${\;}_{92}^{238}$U | |
| D. | Cl-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
; +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$ +NaCl;I→J
+NaCl;I→J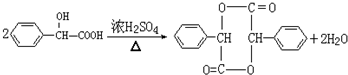 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化钠的分子式:NaCl | |
| B. | 氢氧根离子的电子式: | |
| C. | 氯原子的结构示意图: | |
| D. | 中子数为146、质子数为92的铀(U)原子14692U |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2溶于水成为硅酸 | |
| B. | CO2通入水玻璃中得到白色沉淀 | |
| C. | CO2通入饱和CaCl2溶液能生成白色沉淀 | |
| D. | 硅酸酸性比碳酸弱,所以SiO2不能跟Na2CO3反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有6.02×1023个微粒 | |
| B. | 硫酸的摩尔质量是98g | |
| C. | 等质量的SO2和SO3中所含的硫原子数相等 | |
| D. | 等质量的O2和O3中所含的氧原子数相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com