
如图是制备和研究乙炔性质的实验装置图.下列说法不正确的是( )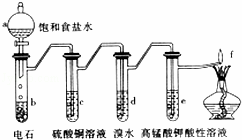
A.制备乙炔的反应原理是CaC2+2H2O→Ca(OH)2+C2H2↑
B.c的作用是除去影响后续实验的杂质
C.d中的有机产物与AgNO3溶液混合能产生沉淀
D.e中的现象说明乙炔不能被高锰酸钾酸性溶液氧化
考点:性质实验方案的设计;常见气体制备原理及装置选择;实验装置综合.
分析:由制备和研究乙炔性质的实验装置图可知,b中饱和食盐水与电石发生CaC2+2H2O→Ca(OH)2+C2H2↑,c中硫酸铜除去杂质硫化氢,d中溴水与乙炔发生加成反应,e中乙炔与高锰酸钾发生氧化反应,最后点燃尾气,以此来解答.
解答: 解:A.b中饱和食盐水与电石发生CaC2+2H2O→Ca(OH)2+C2H2↑,为制备乙炔的反应原理,故A正确;
B.c中硫酸铜除去杂质硫化氢,防止硫化氢对后续实验的影响,故B正确;
C.d中溴水与乙炔发生加成反应生成的有机产物为1,1,2,2﹣四溴乙烷,不能电离出溴离子,则不能与AgNO3溶液反应,故C错误;
D.c中已经排除杂质的干扰,e中乙炔与高锰酸钾发生氧化反应,高锰酸钾溶液褪色可说明乙炔能被氧化,故D错误;
故选CD.
点评:本题考查物质的制备及性质实验的设计,为高频考点,把握实验装置的作用、反应原理为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
不可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
|
| A. | 分别加入碘水,观察颜色反应 |
|
| B. | 分别加热,观察是否生成沉淀 |
|
| C. | 分别滴加浓硝酸 |
|
| D. | 分别灼烧,闻味道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
能在溶液中大量共存的一组离子是 ( )
A . NH4+ 、Ag+ 、PO43-、Cl- B.Fe3+、H+、I-、 HCO3-
C. K+、 Na+、 NO3- 、 MnO4- D.Al3+ 、Mg2+、SO42- 、CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是元素周期表的一部分,针对a~K十一种元素回答下列问题(请用具体化学式回答,否则不给分):
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 2 | a | c | d | e | f | g | |
| 3 | b | h | i | j | k |
(1)这些元素中非金属性最强的单质是 ,最高价氧化物对应水化物酸性最强的是 ,最高价氧化物对应水化物碱性最强的是 。
(2)表中K的氢化物的化学式为 ,它的还原性比j的氢化物还原性 (填“强”或“弱”),它水溶液的酸性比j的氢化物水溶液的酸性 (填“强”或“弱”)。
(3)e单质为 ,其结构式为 。
(4)用电子式表示h与k构成化合物的形成过程
(5)写出i的氧化物与强碱溶液反应的离子方程式
(6)H2和e的单质化合的反应是可逆反应,且该反应正方向放热。将等物质的量的H2、e的单质充入一恒容密闭容器中,在适当条件下反应。下列说法正确的是 (填写选项)。
A.升高温度,不论正反应方向还是逆反应方向速率都加快
B.向上述容器中充入适量Ar气可加快反应速率
C.反应过程中,e的单质的体积分数始终为50%
D.反应器内压强不随时间变化而变化,说明反应到达平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是()
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
查看答案和解析>>
科目:高中化学 来源: 题型:
取100mL Na2CO3 和Na2SO4的混合溶液,加过量BaCl2溶液后得到16.84g 白色沉淀,沉淀用过量稀HNO3 处理质量减少到6.99g,并有气体放出.试计算:
(1)原混合溶液中Na2SO4 的物质的量浓度; L
(2)产生的气体在标准状况下的体积. .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com