
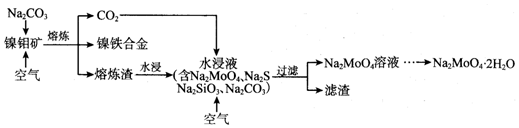

���� �����⾫��MoS2ȼ�գ���Ӧ����ʽΪ2MoS2+7O2$\frac{\underline{\;\;��\;\;}}{\;}$2MoO3+4SO2�����������£�MoO3��Na2CO3��Һ��Ӧ����Ӧ����ʽΪMoO3+CO32-=MoO42-+CO2����Ȼ������Һ�м����������ȥ�ؽ������ӣ���Һ�е�����ΪNa2MoO4������Һ����Ũ������ȴ�ᾧ��Ȼ���ؽᾧ�õ�Na2MoO4.2H2O��
��1����Ʒ����Һ���������������ͨ��Ʒ���У�Ʒ����ɫ�����Ⱥ��ָֻ���ɫ��֤����SO2��
��2��Ԫ�ػ��ϼ����ߣ�����������Ӧ���õ����������Ӧ��ֻ��CԪ�ػ��ϼ����ߣ����ݷ���ʽ�����������ʵ������ٸ���CԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
��3��SiO2��������������������Һ��Ӧ��ˮ��Һ�к�SiO32-��ͨ�������̼����Ӧ���ɹ��������
��4�����������º�̼�ᱵ���ܶȻ��������Һ��̼������ӵ�Ũ�ȣ����ټ����SO42-��ȥ���ʣ�
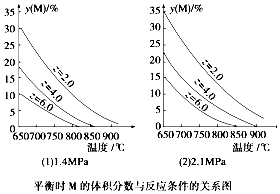
��5�����ٸ���ͼ��������ڻ�ʴ����̼�ֵĸ�ʴ����������С����ʴЧ����ã���õĸ�ʴЧ�����е㴦��
��Ũ������ǿ�����ԣ���ʹ���������γ����ܵ�����Ĥ�����㣻
�۸���ͼʾ���ݷ���̼��������������и�ʴ���������Ũ�ȱ仯�����Բ����ԭ��̼���������еĸ�ʴ�������Կ�������ĸ�ʴ�ٶȣ�����Ũ��������Ũ��������˶ۻ�����ʴ�ٶȺ������ݴ����ʵ�鷽����
��� �⣺��1����Ʒ����Һ�������������������������ڵķ���Ϊ����¯��ͨ��Ʒ���У���Ʒ����ɫ�����Ⱥ��ָֻ���ɫ��֤��¯������SO2����Ʒ�첻��ɫ����¯���в�����SO2��
�ʴ�Ϊ����¯��ͨ��Ʒ���У���Ʒ����ɫ�����Ⱥ��ָֻ���ɫ��֤��¯������SO2����Ʒ�첻��ɫ����¯���в�����SO2��
��2��3FeS2+6Na2CO3+11C+8O2 $\frac{\underline{\;����\;}}{\;}$3Fe+6Na2S+17CO2����Ӧ�л��ϼ����ߵ�Ԫ��ΪCԪ�ػ��ϼ���0������Ϊ+4�ۣ���11C��11CO2�������ϼ۽��͵�Ԫ��ΪFe��S��OԪ�أ�
Fe��+2�۽���Ϊ0�ۣ�����3FeS2��3Fe����S��-1�۽���Ϊ-2�ۣ�����3FeS2��6Na2S��0��0�۽���Ϊ-2�ۣ���8O2��17CO2����CԪ�ػ��ϼ���0������Ϊ+4�ۣ���CO2�����������Ӧ��ֻ��CԪ�ػ��ϼ����ߣ�ÿ����11mol Cʱת�Ƶ���Ϊ44mol��������3mol����Ӧÿת��11mol e-��������$\frac{3}{4}$mol��������������Ϊ$\frac{3}{4}$mol��56g/mol=42g��
�ʴ�Ϊ��CO2��42g��
��3��SiO2��������������������Һ��Ӧ��ˮ��Һ�к�SiO32-��ͨ�������̼������ӦΪSiO32-+CO2+H2O=H2SiO3��+CO32-�������õ��ij���ΪH2SiO3��
�ʴ�Ϊ��H2SiO3��
��4��Ksp��BaMoO4��=4.0��10-8����������Һ��c��MoO42-��=0.4 0mol•L-1��BaMoO4��ʼ����ʱ����Һ�б����ӵ�Ũ��Ϊ��c��Ba2+��=$\frac{4.0��1{0}^{-8}}{0.4mol/L}$=1��10-7mol/L��Ksp��BaCO3��=1��10-9����Һ��̼������ӵ�Ũ��Ϊ��c��CO32-��=$\frac{1.0��1{0}^{-9}}{1..0��1{0}^{-7}}$mol/L=1.0��10-2mol/L��ԭ��Һ��c��CO32-��=0.10mol•L-1��̼������ӵ�ȥ����Ϊ��1-$\frac{1.0��1{0}^{-2}}{0.1}$��100%=1-10%��90%��
�ʴ�Ϊ��90%��
��5���ٸ���ͼʾ��֪���������ơ��¹��ἡ����Ũ�����ʱ����ʴ������С����ʴЧ����ã���Ũ�ȱ�Ϊ1��1��
�ʴ�Ϊ��1��1��
�ڵ������Ũ�ȴ���90%ʱ����ʴ���ʼ���Ϊ�㣬ԭ���dz�����Ũ�������ǿ�����ԣ���ʹ���ۻ�������ʴ���ã�
�ʴ�Ϊ��������Ũ�������ǿ�����ԣ���ʹ���ۻ���
����ͼʾ���ݿ�֪��̼���������еĸ�ʴ�������Կ�������ĸ�ʴ�ٶȣ�����Ũ��������Ũ��������˶ۻ�����ʴ�ٶȺ��������ʵ��֤���������ۿ����Ϊ��������������Һ�м��������Ȼ��Ƶȿ������Ȼ��̼�ظֵĸ�ʴ�������Լӿ죬
�ʴ�Ϊ��Cl-������̼�ֵĸ�ʴ��SO42-������̼�ֵĸ�ʴ��������������Һ�м��������Ȼ��Ƶȿ������Ȼ��̼�ظֵĸ�ʴ�������Լӿ죮
���� ���⿼�����Ʊ������ƾ���ķ��������ؿ���������ۺ�Ӧ��֪ʶ��������ע���������ͼʾ�ǽ���ؼ���ע������ܽ�ƽ�����������Ũ�ȼ�Ĺ�ϵ��Ϊ�״��㣬�����Ѷ��еȣ�


 Ӧ�����������Ĵ���ѧ������ϵ�д�
Ӧ�����������Ĵ���ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�ɶ��и�һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
15 g A���ʺ�10.5 g B������ȫ��Ӧ������7.2 g C���ʣ�1.8 g D���ʺ�0.3 mol E���ʣ���E��Ħ������Ϊ�� ��
A��16.5 g��mol-1 B��85 g��mol-1 C��27.5 g��mol-1 D��55 g��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | a+b��c+d | |
| B�� | ͬ��ͬѹʱ������z��ƽ��ʱQ������������� | |
| C�� | ͬѹͬzʱ�������¶ȣ�����ƽ��Ħ���������� | |
| D�� | ͬ��ͬzʱ������ѹǿ��ƽ��ʱQ�����ʵ���Ũ�ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ�ͽ���ı�������Ϊ�Ƿ��ܲ��������ЧӦ | |
| B�� | K2Cr2O7��Һ���������ܴ����ͬһҩƷ���� | |
| C�� | �ô���������ϸ���Լ�ƿ��������� | |
| D�� | CH4��C2H4�����ڳ���Σ��Ʒ�е���ȼ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ӡˢ��·�壺Fe3++Cu�TCu2++Fe2+ | |
| B�� | �����ʵ�����Ba��OH��2��NH4HSO4��ϡ��Һ�з�Ӧ��Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O | |
| C�� | Ca��OH��2��Һ������Ca��HCO3��2��Һ��Ӧ��Ca2++2HCO3-+2OH-�T2CaCO3��+2H2O+CO32- | |
| D�� | ���Ʊ�����ˮ�м���ʯ��ʯ�������Һ��HClOŨ�ȣ�CaCO3+2Cl2+H2O�TCa2++2Cl-+CO2��+2H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com