


科目:高中化学 来源:不详 题型:单选题
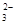 +O2+xOH—
+O2+xOH— +2H2O,
+2H2O,| A.每生成1mol Fe3O4,反应转移的电子总数为3mol ; |
| B.x="6" |
| C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol; |
| D.Fe2+和S2O32—-都是还原剂; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CHCl3 | B.CH3CH2Br |
| C.CH2BrCH2CH2OH | D.CH3CH2OH |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4和FeS2是氧化剂,FeS2是还原剂 |
| B.5 mol FeS2发生反应,有21 mol e—转移 |
| C.Cu2S既是氧化产物又是还原产物 |
| D.产物中的SO42-有一部分是氧化产物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NaH中H的化合价为+1价,是氧化剂 |
| B.在该反应中H2O 为还原剂 |
| C.在该反应中NaH 为还原剂 |
D.该反应中电子转移的方向和数目可以表示为: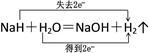 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③ | B.②①③ | C.③②① | D.③①② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2S+2HNO3=S↓+2NO2↑+2H2O |
| B.CuO+2HNO3=Cu(NO3)2+H2O |
C.4HNO3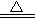 4NO2↑+O2↑+2H2O 4NO2↑+O2↑+2H2O |
| D.3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5∶3 | B.5∶4 | C.1∶1 | D.3∶5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com