
| 化合物 | 甲烷 | 乙烷 | 丙烷 | 正丁烷 | 异丁烷 | 异戊烷 |
| 燃烧热 (kJ•mol-1) | 891.0 | 1560.8 | 2221.5 | 2878.0 | 2869.6 | 3531.3 |
| A. | 正丁烷?异丁烷△H<0 | |
| B. | 乙烷燃烧的热化学方程式为:2C2H6(g)+7O2(g)═CO2(g)+6H2O(g)△H=-1560.8 kJ•mol-1 | |
| C. | 正戊烷的燃烧热数值小于3531.3 kJ•mol-1 | |
| D. | 相同质量的烷烃,随碳原子数增加,燃烧放出的热量增多 |
分析 A、根据正丁烷和异丁烷的燃烧热判断能量高低;
B、乙烷的燃烧热为1560.8KJ/mol,说明完全燃烧1mol乙烷生成二氧化碳和液态水时会放出1560.8KJ的热量;
C、正丁烷的燃烧热和其同分异构体的燃烧热相近,比含有支链的同分异构体高点,以此来分析正戊烷的燃烧热;
D、相同质量的烷烃,燃烧放热多少和碳的质量分数有关.
解答 解:A、因为正丁烷的燃烧热比异丁烷大,所以等量的正丁烷能量比异丁烷大,则正丁烷?异丁烷放热即△H<0,故A正确;
B、根据乙烷燃烧热的含义:完全燃烧1mol乙烷生成二氧化碳和液态水时会放出1560.8KJ的热量,所以热化学方程式为2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l);△H=-3121.6kJ/mol,故B错误;
C、正戊烷和2-甲基丁烷互为同分异构体,由表格中正丁烷、异丁烷的燃烧热比较可知,则互为同分异构体的化合物,支链多的燃烧热小,则正丁烷的燃烧热大于2-甲基丁烷,即正戊烷的燃烧热大约在3540KJ/mol左右,且大于3531.3KJ/mol,故C错误;
D、相同质量的烷烃,碳的质量分数越小,燃烧放热越多,故D错误.
故选A.
点评 本题是一道关于化学反应中的能量变化以及燃烧热概念的题目,可以根据所学知识进行回答,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NaCl溶液中有杂质Na2SO4(适量的BaCl2溶液) | |
| B. | FeSO4溶液中有杂质CuSO4 (Fe粉) | |
| C. | CO2气体中有少量CO(灼热的氧化铜) | |
| D. | SO2气体中有少量HCl气体(NaOH溶液) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、C1O-、C1O3-三种含氯元素的离子,其中C1O-、C1O3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A | 1使溴的四氯化碳溶液褪色;②比例模型为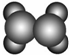 ;③能与水在一定条件下反应生成C ;③能与水在一定条件下反应生成C |
| B | 1C、H两种元素组成;②球棍模型为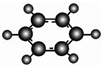 |
| C | ①由C、H、O三种元素组成;②能与Na反应,但不能与NaOH溶液反应;③能与D反应生成相对分子质量为100的酯 |
| D | ①由C、H、O三种元素组成;②球棍模型为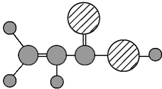 |
 +HO-NO2$→_{△}^{浓硫酸}$
+HO-NO2$→_{△}^{浓硫酸}$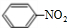 +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 酸 | HCN | HAc | HF | H2SO3 |
| Ka | 4.9×10-10 | 1.75×10-5 | 3.5×10-4 | K1=1.5×10-2 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液由溶质和溶剂组成,所以每种溶液里只有两种物质 | |
| B. | 硫酸钠溶液能导电是因为溶液中含有较多自由移动的离子 | |
| C. | 配置0.09%的生理盐水的一般步骤是计算、称量和溶解 | |
| D. | 在稀释浓硫酸时,一定要把浓硫酸沿器壁慢慢注入水中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com