
| A. | 液氯 | B. | 淀粉 | C. | 硝酸钾 | D. | 液态氯化氢 |
科目:高中化学 来源: 题型:解答题
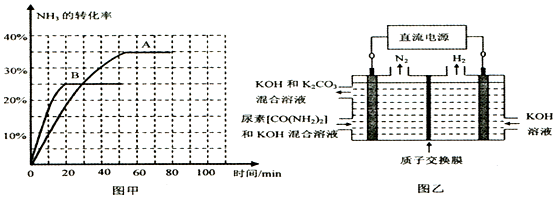
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验A | 实验B | |
| 操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液. | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水. |
| 现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=l的溶液:Ba2+、Al3+、Cl-、SO42- | |
| B. | 能使酚酞试液变红的溶液:Na+、K+、HCO3-、I- | |
| C. | c(OH-)/c(H+)=10-12的溶液:NH4+、Cu2+、NO3-、Cl- | |
| D. | 含有0.1mol/LFe(NO3)2的溶液:H+、Mg2+、SCN-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | b中物质 | b中现象 | 结论或解释 | |
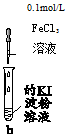 | A | Mg(OH)2悬浊液 | 有红棕色胶体产生 | 发生反应:Fe3++3OH-═Fe(OH)3(胶体) |
| B | Cu粉 | 溶液变蓝,试管底部有固体 | 溶液变蓝的原因是:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C | 5%H2O2溶液 | 有气泡生成 | 该气体为氯气,双氧水强氧化性氧化Cl-产生 | |
| D | 饱和NaHCO3溶液 | 有气泡生成,且试管底部有固体 | 发生反应:Fe3++3HCO3-═Fe(OH)3+3CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁和铜在自然界中主要以游离态的形式存在 | |
| B. | 工业上在高温下用CO还原含Fe2O3的铁矿石炼铁 | |
| C. | 常温下铁与浓硫酸不反应 | |
| D. | 用激光照射硫酸铜溶液可观察到丁达尔现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符合分子通式CnH2n+2的烃一定都是烷烃,分子中均只含单键 | |
| B. | 通过石油裂化可以得到多种气态短链烃,其中包括重要化工原料 | |
| C. | 苯能使溴水褪色,说明苯环结构中含有碳碳双键 | |
| D. | 乙醇可以被氧气氧化成乙酸,但乙酸无法再被氧气氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 | 结论 |
| A | 向FeBr2溶液中加入少量氯水,再加 CCl4振荡 | CCl4层无色 | Fe2+的还原性强于Br- |
| B | 向盐酸中滴入少量NaAlO2溶液 | 无明显现象 | AlO2-与H+未发生反应 |
| C | 向某溶液里滴加NaOH溶液并将湿润的红色石蕊试纸罝于试管口 | 试纸颜色无 明显变化 | 原溶液中无NH4+ |
| D | 常温下,测定等物质的量浓度的 Na2CO3和Na2SO3溶液的pH | 前者的pH 比后者的大 | 元素非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将2mL 0.5mol•L-1Na2SiO3溶液滴入稀盐酸中制得H2SiO3胶体,所含胶粒数为0.001NA | |
| B. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| C. | 标准状况下,20g D2O分子中所含中子数为10NA | |
| D. | 将1mol Cl2通入水中,HClO、Cl-、ClO-粒子数之和为2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com