
将1.000gFeC2O4·2H20固体样品放在热重分析仪中进行热重分析,測得其热重分析曲线(样品质量随温度变化的曲线)如下图所示: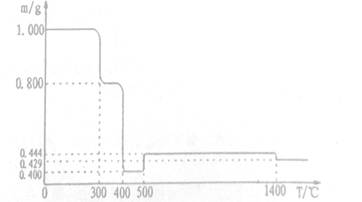
已知:①草酸盐受热分解易放出碳的氧化物。②5000C之前,该热重分析仪的样品池处于Ar气气氛中,5000C时起,样品池与大气相通。完成下列填空:
(1)3000C时是样品脱水的过程,试确定3500C时样品是否脱水完全_____ (填“是"或否“),判断的理由是____(要求写出推算过程)。
(2 ) 4000C时发生变化的化学方程式是_______。
(3) 将6000C时样品池中残留的固体隔绝空气冷却至室温,再向该固体中加入一定量的稀盐酸刚好完全溶解,用pH试纸测得所得溶液的PH=3,其原因是____(用离子方程式回答):向该溶液中滴加适量NaOH溶液生成红褐色沉淀,測得此时溶液中铁元索的离子浓度为4.0x10-11mol/L,则此时溶液的pH=_______(已知:Ksp[Fe(OH)2]=8.0×10-16,Ksp[Fe(OH)3]=4.0×10-38)
(4) 将15000C时样品池中残留的固体隔绝空气冷却后,用稀盐酸溶解得一棕黄色溶液。取少量该溶液滴加KSCN,溶液显红色;另取少量该溶液滴加K3[Fe(CN)6)(铁氰化钾)溶液,产生特征蓝色沉淀。试写出图中14000C时发生反应的化学方程式_________ ,产生特征蓝色沉淀的离子反应方程式______。
(1)是(2分)(2)FeC2O4 FeO+CO↑+CO2↑(2分)
FeO+CO↑+CO2↑(2分)
(3)Fe3++3OH- Fe(OH)3+3H+(2分) ; 5(2分) (4)6Fe2O3
Fe(OH)3+3H+(2分) ; 5(2分) (4)6Fe2O3 4Fe3O4+O2↑(2分);
4Fe3O4+O2↑(2分);
3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓或K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓(2分)
解析试题分析:(1)样品分解的方程式是
FeC2O4·2H2O FeC2O4·(2-n)H2O+nH2O
FeC2O4·(2-n)H2O+nH2O
180g 18n
1.000g (1.000g-0.800g)
解得n=2,所以样品已经完全分解
(2)400℃时固体又减少了0.800g-0.400g=0.400g
根据铁原子守恒可知,400℃铁的含量应该是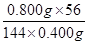 =
= ,因此该化合物是氧化亚铁,其化学式是FeO,所以反应的化学方程式是FeC2O4
,因此该化合物是氧化亚铁,其化学式是FeO,所以反应的化学方程式是FeC2O4 FeO+CO↑+CO2↑。
FeO+CO↑+CO2↑。
(3)600℃样品中铁元素的含量是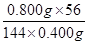 =0.70,因此该固体是氧化铁。氧化铁溶于盐酸生成氯化铁,铁离子水解溶液显酸性,其离子方程式是Fe3++3OH-
=0.70,因此该固体是氧化铁。氧化铁溶于盐酸生成氯化铁,铁离子水解溶液显酸性,其离子方程式是Fe3++3OH- Fe(OH)3+3H+。根据氢氧化铁的溶度积常数可知,当溶液中铁离子的离子浓度为4.0x10-11mol/L时,溶液中c(OH-)=
Fe(OH)3+3H+。根据氢氧化铁的溶度积常数可知,当溶液中铁离子的离子浓度为4.0x10-11mol/L时,溶液中c(OH-)=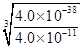 =10-9mol/L,所以溶液中c(H+)=10-5mol/L,因此pH=5。
=10-9mol/L,所以溶液中c(H+)=10-5mol/L,因此pH=5。
(4)另取少量该溶液滴加K3[Fe(CN)6)(铁氰化钾)溶液,产生特征蓝色沉淀,这说明溶液中还有亚铁离子生成。因此1400℃时氧化铁分解生成了四氧化三铁,反应的化学方程式是6Fe2O3 4Fe3O4+O2↑;产生特征蓝色沉淀的离子反应方程式3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓或K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓。
4Fe3O4+O2↑;产生特征蓝色沉淀的离子反应方程式3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓或K++Fe2++[Fe(CN)6]3-=KFe[Fe(CN)6]↓。
考点:考查醋酸盐铁分解的有关计算、离子检验以及方程式的书写等


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源: 题型:填空题
常见金属单质A、B和非金属单质C、D以及它们化合物之间的转化关系如下。F、J既能溶于强酸M又能溶于强碱N,Z的摩尔质量为198 g·mol-1,且其中各元素的质量比为:钾:金属B:氧=39:28:32。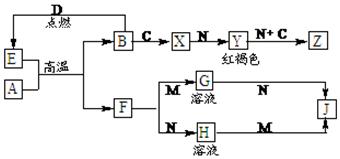
请回答下列问题:
(1)C的化学式为 ,Z的化学式为 。
(2)写出检验X中阳离子的方法 。
(3)写出E和A在高温下反应的化学方程式为 。
(4)写出A和N反应的离子方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下:
(1)滤液A所含溶质属于盐的是___________________。
(2)检验滤液B中是否还含有铁元素的方法为:_______________________________________
____________________________________________________________(注明试剂、现象)。
(3)将滤液B中的铝元素以沉淀形式析出,最佳试剂应选_____________(填代号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
(4)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填代号)。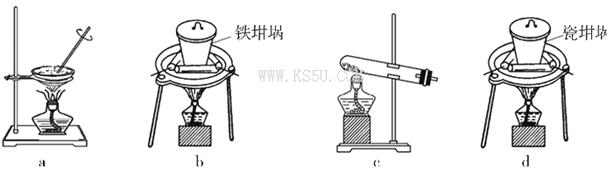
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
从铝土矿(主要成分是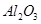 ,含
,含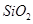 、
、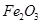 、MgO等杂质)中提取两种工艺品的流程如下:
、MgO等杂质)中提取两种工艺品的流程如下: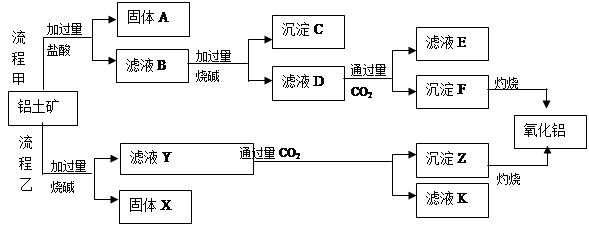
请回答下列问题:
(1)流程乙加入烧碱后的离子方程式为_________________________________________.
(2)固体A的应用_________________________________________.(两点)
(3)滤液D与少量CO2反应的离子方程式为__________________________________,
向该滤液K中加入足量石灰水的离子方程式是________
(4)流程乙制氧化铝的优点是所用的试剂较经济,缺点是__________________________
(5)已知298K时, 的溶度积常数
的溶度积常数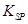 =10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的PH最小为_______.
=10-11,取适量的滤液B,加入一定量的烧碱恰使镁离子沉淀完全,则溶液的PH最小为_______.
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
镁铝尖晶石(MgAl2O4)常做耐火材料。共沉淀制备尖晶石的方法是:用AlCl3和MgCl2的混合溶液(用a表示)与过量的氨水(用b表示)反应,再将得到的沉淀高温焙烧。完成下列填空:
(1)为使Mg2+、Al3+同时生成沉淀,应该把 (填“a”或“b”)滴入另一溶液中。
(2)将上述制备反应中部分元素的简单离子:Al3+、Cl–、Mg2+、H+、O2–按半径由大到小的顺序排列
(用离子符号表示)。
(3)AlCl3与氨水反应的反应物和生成物中,属于离子化合物的电子式是 ,属于难溶物的电离方程式 。
(4)不能说明氧元素的非金属性比氮元素强的事实是_________。
a. H2O比NH3稳定 b. 共用电子对偏向:H-O>H-N
c. 沸点:H2O>NH3 d. NO中氮是+2价,氧是-2价
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法。
(1)氯化铝融盐电解法需要先制纯氧化铝。以铝土矿(主要成分为Al2O3,含有少量Fe2O3、SiO2等杂质)为原料通过以下途径提纯氧化铝:
①依次写出X、Y的成分 , 。
②如图所示在实验室中进行过滤,操作中的两处错误分别是 ; 。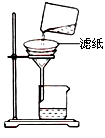
(2)制备无水氯化铝的反应为:2Al2O3+6Cl2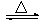 4AlCl3+3O2
4AlCl3+3O2
③为促进该反应的进行,实际生产中需加入焦炭,其原理是 。
④加入焦炭后的化学反应可表示为Al2O3+C+Cl2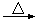 AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由 。
AlCl3+X↑,为确定气体X是否是混合气体,某同学将X依次通过灼热的氧化铜和澄清的石灰水,再根据现象判断。该操作是否正确?(填正确、不正确或无法判断) ,请说明理由 。
(3)现在工业上通常用电解熔融氧化铝方式制取铝,理论上生产1吨铝消耗的氧化铝的质量_________
(填“大于”、“小于”、“等于”)氯化铝质量。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题。
(1)碳酸氢钠的化学式是 ,俗称 。
(2)碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为 。等物质的量的碳酸钠和碳酸氢钠与足量盐酸反应时生成CO2的量,前者 后者(填“>”、“<”或“=”)。
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(15分)银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下: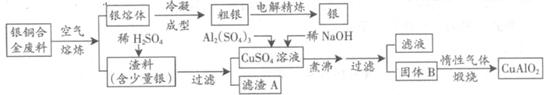
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)电解精炼银时,阴极反应式为 ;滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为 。
(2)固体混合物B的组成为 ;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为 。
(3)完成煅烧过程中一个反应的化学方程式: CuO+ Al2O3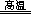 CuAlO2 + ↑。
CuAlO2 + ↑。
(4)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为 mol CuAlO2,至少需要1.0mol?L—1的Al2(SO4)3溶液 L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是 、过滤、洗涤和干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
将5.1g镁铝合金投入过量盐酸中充分反应,得到500mL溶液和5.6L标准状况下的H2。计算:
(1)合金中镁和铝的质量之比;
(2)所得溶液中Mg2+的物质的量浓度。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com