
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 分子式为C5H12O的有机物,它的同分异构体中,经氧化可生成醛,该有机物属于醛,且连接羟基的碳原子上含有2个氢原子,确定C5H12的同分异构体,-OH取代C5H12中甲基上的H原子,此确定醇的结构简式.
解答 解:分子式为C5H12O的有机物,它的同分异构体中,经氧化可生成醛,该有机物属于醛,且连接羟基的碳原子上含有2个氢原子,确定C5H12的同分异构体,-OH取代C5H12中甲基上的H原子,
C5H12的同分异构体有:CH3CH2CH2CH2CH3、CH3CH(CH3)CH2CH3、(CH3)4C,
当烷烃为CH3CH2CH2CH2CH3,-OH取代甲基上的H原子有1种结构,
当烷烃为(CH3)2CHCH2CH3,-OH取代甲基上的H原子有2种结构,
当烷烃为(CH3)4C,-OH取代甲基上的H原子有1种结构,
C5H12O的同分异构体中可以氧化为醛的醇有4种.
故选C.
点评 本题考查同分异构体的书写,难度较大,注意能被氧化成醛必须是与羟基相连的碳原子上含有至少2个氢原子.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:选择题
| A. | 太阳能光电池的主要成份是单质硅 | |
| B. | 核电站泄漏的放射性碘-131(${\;}_{53}^{131}$I)、铯-137(${\;}_{55}^{137}$Cs)互称同位素 | |
| C. | 汽车尾气污染物中含有的氮氧化物,是汽油不完全燃烧造成的 | |
| D. | 某雨水样品放置一段时间后pH由4.68变为4.28,是因为吸收了CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
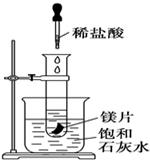 如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10mL盐酸于试管中,试回答下列问题:
如图所示,把试管放入盛有25℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10mL盐酸于试管中,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 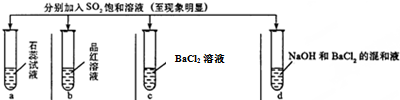 | ||||
| 记录 | A | 无色 | 无色 | 无现象 | 无色溶液 |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 无色溶液 | 无色溶液 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,4.6g NO2或N2O4气体中所含原子总数均为0.3NA | |
| B. | 标准状况下,22.4 mL Br2所含的分子数为0.001NA | |
| C. | 标准状况下,22.4L的Cl2与1mol Fe充分反应,转移的电子数为3NA | |
| D. | 100 mL 0.1 mol•L-1的H2SO3溶液中,电离出的H+总数为0.02 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com