
| A. | NaCl的摩尔质量是58.5g | |
| B. | 将40g氢氧化钠溶解在1L水中可配制物质的量浓度为1mol/L的氢氧化钠溶液 | |
| C. | 气体摩尔体积指lmol任何气体所占的体积约为22.4L | |
| D. | 10毫升1mol/L氯化铝溶液与50毫升3mol/L氯化钠溶液中所含氯离子物质的量浓度相等 |
分析 A.摩尔质量的单位是g/mol;
B.溶液的体积不等于容积的体积;
C.气体摩尔体积与状态有关,不一定是22.4L/mol;
D.离子的物质的量浓度=溶质的物质的量浓度×一个溶质中含有离子的个数,与溶液的体积无关.
解答 解:A.NaCl的摩尔质量是58.5g/mol,故A错误;
B.40g氢氧化钠的物质的量为1mol,但溶液的体积不等于1L,因此所得氢氧化钠溶液的浓度不是1mol/L,故B错误;
C.气体摩尔体积与状态有关,不一定是22.4L/mol,因此lmol任何气体所占的体积不一定约为22.4L,故C错误;
D.1mol/L氯化铝溶液中氯离子的浓度为1mol/L×3=3mol/L,3mol/L氯化钠溶液中氯离子的浓度为3mol/L×1=3mol/L,故D正确;
故选D.
点评 本题考查较为全面,涉及摩尔质量、气体的摩尔体积、物质的量浓度的计算与理解,题目难度不大,注意溶液中溶质离子的浓度与溶液体积无关,只取决于物质电离出的离子的数目多少与溶质的浓度.


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:选择题
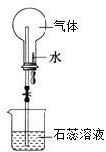
| A. | 烧瓶中的溶液呈红色,则原气体一定是SO2 | |
| B. | 形成喷泉的原因是烧瓶内压强小于外界大气压 | |
| C. | 烧瓶中的溶液呈蓝色,则原气体一定属于是碱类物质 | |
| D. | 若将石蕊改成氢氧化钠,则CO、CO2均能形成喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用前检查是否漏水 | B. | 溶液未冷却即注入容量瓶中 | ||
| C. | 容量瓶可长期存放溶液 | D. | 在容量瓶中直接溶解固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 金属 | 实验操作 | 实验现象 |
| 甲 | ①取少量粉末,加入过量浓硝酸 ②向上述溶液中加入几滴NaCl溶液 | 粉末溶解,有红棕色气体产生 有白色沉淀生成 |
| 乙 | ③取少量粉末,加入足量NaOH溶液 ④向上述溶液中逐滴加入稀盐酸 ⑤继续加入过量的稀盐酸 | 粉末溶解,有气泡产生 有白色沉淀生成 白色沉淀溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂混合不一定发生氧化还原反应 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加且有单质生成的反应一定属于氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应必然伴随能量的变化 | |
| B. | 我国目前使用的主要能源是化石能源 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 化学反应一定有化学键的断裂与形成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol 18O含有的中子数为10NA | |
| B. | 22.4L甲烷气体中所含分子数目为NA | |
| C. | 1L 0.1mol•L-1NH4Cl 溶液中NH4+数目为 0.1NA | |
| D. | 1L pH=1的醋酸溶液中,CH3COOH分子的数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com