
| A��ƽ��ʱ���ס�����������A��B�����ʵ���֮�Ȳ���� |
| B����ƽ��ʱ���ס�����������A�����ʵ�����ȣ���x=2 |
| C��ƽ��ʱ����A���������Ϊ40% |
| D����ƽ��ʱ�������е�ѹǿ����ȣ�����������ѹǿ֮��Ϊ5��8 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��28g N2��28g CO�����ķ���������NA |
| B��32g O3��32g O2�����ķ���������NA |
| C��28g CO��44g CO2��������ԭ��������2NA |
| D��98g H2SO4��98g H3PO4��������ԭ��������4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ���� | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
| pH | 11.6 | 9.7 | 10.3 | 4.0 |
| A������ˮ�м���NaHCO3������������ˮ�д������Ũ�� |
| B��������Һ�У�ˮ�ĵ���̶�������NaClO |
| C�������£���ͬ���ʵ���Ũ�ȵ�H2SO3��H2CO3��HClO��pH������H2SO3 |
| D��NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc��Na+����c��H+����c��HSO3-����c��SO32-����c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
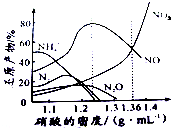 ������M���ĸ�ʴ����Ϊ������Ӧ��M-ne-��Mn+��������ʴ��ɺܴ�ľ�����ʧ������������Ȼ�ֺ������и����ĸ�ʴ��Ϊ���أ�Ѱ���ֹ������ʴ�ķ��������ش�
������M���ĸ�ʴ����Ϊ������Ӧ��M-ne-��Mn+��������ʴ��ɺܴ�ľ�����ʧ������������Ȼ�ֺ������и����ĸ�ʴ��Ϊ���أ�Ѱ���ֹ������ʴ�ķ��������ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| A�����廯������Һ�м����廯����Һ���廯����Ksp��С |
| B����c�����Һ�м���0.1mol?L-1AgNO3����c��Br-����С |
| C�������¶ȿ���ʵ��c�㵽b���ת�� |
| D��ͼ��b���Ӧ���Dz�������Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
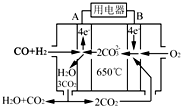 �о�NO2��SO2��CO�ȴ�����Ⱦ����IJ���������������Ҫ���壮
�о�NO2��SO2��CO�ȴ�����Ⱦ����IJ���������������Ҫ���壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| T/�� | 200 | 300 | 400 |
| H2��������� | a1 | a2 | 25% |
| A��a1��a2 |
| B������Ӧ��400���½��У���ﵽƽ��ʱN2��ת����Ϊ20% |
| C������Ӧ��300���½��У���ﵽƽ��ʱ��Ӧ�ų�������Ϊ23.1 kJ |
| D������Ӧ��200���½��У���ﵽƽ��ʱN2���������Ϊ50% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
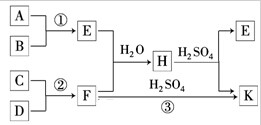
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com