
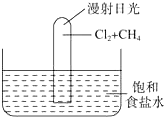
 如图所示实验,试推测可能观察到的现象是:
如图所示实验,试推测可能观察到的现象是:分析 甲烷与氯气在光照条件下发生取代反应生成CH3Cl(气体)、CH2Cl2、CHCl3、CCl4、HCl,氯气逐渐减少甚至消失,氯气的颜色逐渐变浅或消失;反应后有油状液滴(二氯甲烷、三氯甲烷与四氯甲烷)出现;反应过程中气体的体积减小,导致试管内的压强低于外界大气压;氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,溶液的pH变小.
解答 解:甲烷与氯气在光照条件下发生取代反应:甲烷与氯气发生取代反应生成一氯甲烷、二氯甲烷、三氯甲烷、四氯甲烷和HCl,该反应为:CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl,CH3Cl+Cl2$\stackrel{光照}{→}$CH2Cl2+HCl;CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl;CHCl3+Cl2$\stackrel{光照}{→}$CCl4+HCl,生成CH3Cl(气体)、CH2Cl2、CHCl3、CCl4、HCl,随着氯气浓度的变小气体颜色变浅,反应生成的氯化氢极易溶于水,水位沿试管上升,反应后有油状液滴(二氯甲烷、三氯甲烷与四氯甲烷)出现;氯化氢溶于水后溶液中氯离子浓度增大,导致氯化钠固体析出,
故答案为:黄绿色气体变浅;试管内壁附着油状液滴;水位沿试管上升;溶液中有沉淀生成.
点评 本题考查了甲烷的取代反应,题目难度不大,解答本题要掌握各种物质的性质和压强等方面的内容,只有这样才能对相关方面的问题做出正确的判断.


科目:高中化学 来源: 题型:选择题
| A. | 塑料、人造纤维和合成橡胶都属于有机高分子化合物 | |
| B. | 食品透气袋里放入盛有硅胶和铁粉的小袋,可防止食物受潮、氧化变质 | |
| C. | Na2FeO4能与水缓慢反应生成Fe(OH)3和O2,可以作为饮用水的消毒剂和净化剂 | |
| D. | 草木灰和铵态氮肥不能混合使用,是因为NH4++HCO3-═CO2↑+H2O+NH3↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
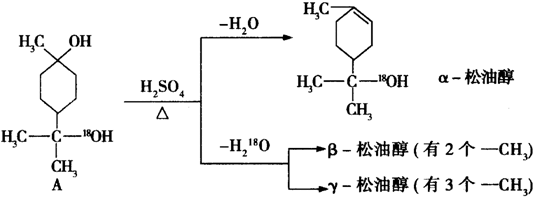
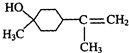 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$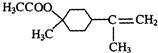 +H2O.
+H2O.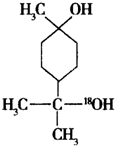 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$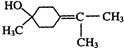 +H218O,该反应的反应类型是消去反应.
+H218O,该反应的反应类型是消去反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
| A. | 在0~1、1~2、2~3、3~4、4~5 min时间段中,反应速率最大的时间段是4 一5 min,因为在此段时间内反应放出的热量较多 | |
| B. | 在2一3min时间段内,用盐酸的浓度变化表示的反应速率为0.lmol/(L•min) | |
| C. | 在该稀盐酸中分别加入等体积的蒸馏水、Na2SO4溶液或Na2CO3溶液都能减缓反应速率且不减少产生氢气的量 | |
| D. | 为了加快该化学反应速率,可以向其中加入NaCl固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A. | 反应开始20 s内以二氧化氮表示的平均反应速率为0.00125 mol/L•s | |
| B. | 80 s时向容器中加入0.32 mol氦气,同时将容器扩大为 4 L,则平衡将不移动 | |
| C. | 当反应达到平衡后,若缩小容器的体积,平衡向生成N2O4方向移动,气体的颜色变深 | |
| D. | 若其它条件不变,起始投料改为0.40 mol N2O4,相同条件下达平衡,则各组分含量与原平衡体系对应相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. ,A2C2的结构式:H-O-O-H.
,A2C2的结构式:H-O-O-H. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 将A、B组成原电池时,A为正极 | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 将A和B用导线相连接,一同放入CuSO4溶液中,B的表面有红色的铜析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H三种核素的性质不同 | |
| B. | 16O2、18O2彼此是同位素 | |
| C. | 14N、14C两种核素的中子数相同,质子数不同 | |
| D. | 白磷与红磷是磷元素的两种同素异形体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com