
(16分)氢是一种理想的绿色清洁能源,氢气的制取与储存是氢能源利用领域的研究热点。 利用FeO/Fe3O4循环制氢,已知:
H2O(g)+3FeO(s) Fe3O4(s) + H2(g) △H=a KJ/mol (Ⅰ)
Fe3O4(s) + H2(g) △H=a KJ/mol (Ⅰ)
2Fe3O4(s)=6FeO(s) + O2(g) △H=b KJ/mol (Ⅱ)
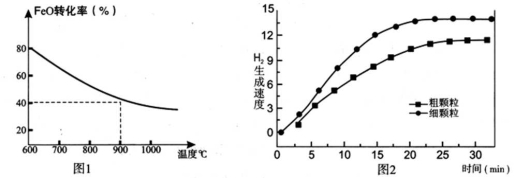
下列坐标图分别表示FeO的转化率(图1)和一定温度时,H2生成速率[细颗粒(直径0.25 mm),粗颗粒(直径3 mm)](图2)。
(1)反应:2H2O(g)=2H2(g) + O2(g) ΔH= (用含a、b代数式表示);
(2)在上述循环制氢的过程中FeO的作用是: ;
(3)900°C时,在两个体积均为2L密闭容器中分别投入0.60molFeO和0.20mol H2O(g),甲容器用细颗粒FeO,乙容器用粗颗粒FeO。
①用细颗粒FeO和粗颗粒FeO时,H2生成速率不同的原因是: ;
②用细颗粒FeO时,H2O (g)的转化率比用粗颗粒FeO时H2O(g)的转化率 (填“大”或“小”或“相等”);
③求此温度下该反应的平衡常数K(写出计算过程)。
(4)在坐标图3中画出在1000°C、用细颗粒FeO时,H2O(g)转化率随时间变化示意图(进行相应的标注):
(1)(2a+b)kJ/mol (2分)(无kJ/mol或“2a+bkJ/mol”扣1分,其他不给分)
(2)作催化剂(2分)
(3)①细颗粒FeO表面积大,与H2的接触面大,反应速率加快;
(3分)(“增大接触面、加快反应速率”、“接触面越大,反应速率越快”等合理表达给3分;答“增大反应物浓度”、“FeO的量增加,反应速率加快”给1分);
②相等(2分)(答“等于”、“=”给1分)
③(4分)【解析】
900℃时,达到平衡FeO转化的量为:n(FeO)=0.60mol×40%=0.24mol,
H2O(g)+3FeO(s) Fe3O4(s)+ H2(g)
Fe3O4(s)+ H2(g)
开始(mol):0.2 0.6 0 0
转化(mol):0.08 0.24 0.08 0.08
平衡(mol):0.12 0.36 0.08 0.08
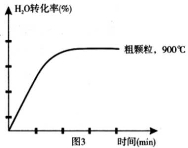
K= =0.6
=0.6
(4)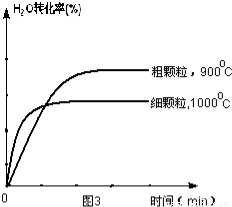 (3分)
(3分)
【解析】
试题分析:(1)已知H2O(g)+3FeO(s) Fe3O4(s)+H2(g)△H=akJ/mol(Ⅰ),2Fe3O4═6FeO(s)+O2g△H=bkJ/mol (Ⅱ),利用盖斯定律,将(Ⅰ)×2+(Ⅱ)可得2H2O(g)═2H2(g)+O2(g)△H=(2a+b)kJ/mol;
Fe3O4(s)+H2(g)△H=akJ/mol(Ⅰ),2Fe3O4═6FeO(s)+O2g△H=bkJ/mol (Ⅱ),利用盖斯定律,将(Ⅰ)×2+(Ⅱ)可得2H2O(g)═2H2(g)+O2(g)△H=(2a+b)kJ/mol;
(2)氧化亚铁在反应前后不变,因此起到催化剂作用;
(3)①因细颗粒FeO表面积大,固体的表面积越大,与氢气的接触面越大,则反应速率越大;
②固体的表面加大小与平衡移动无关,则平衡状态相同,转化率相等;
③由图象可知900℃时,达到平衡FeO转化的量为:n(FeO)=0.60mol×40%=0.24mol
H2O(g)+3FeO(s) Fe3O4(s)+ H2(g)
Fe3O4(s)+ H2(g)
开始(mol):0.2 0.6 0 0
转化(mol):0.08 0.24 0.08 0.08
平衡(mol):0.12 0.36 0.08 0.08
K=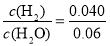 =0.67
=0.67
(4)由图1可知,升高温度,FeO的转化率降低,说明正反应为放热反应,升高温度,反应速率增大,但反应物的转化率降低,则图象为
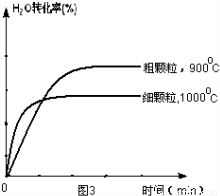 。
。
考点:考查盖斯定律的应用、外界条件对平衡状态的影响以及平衡状态的计算等


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源:2015届广东省佛山市高三9月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.Na2O2能与CO2反应,可用作呼吸面具的供氧剂
B.SiO2有导电性,可用于制备光导纤维
C.硅胶常用作实验室和食品、药品等的干燥剂,也可作催化剂载体
D.小苏打是一种膨松剂,可用于制作馒头和面包
查看答案和解析>>
科目:高中化学 来源:2015届广东省中山市等五校联考高三第一学期化学试卷(解析版) 题型:填空题
(8分)1814年戴维发现了一氯化碘(ICl)、三氯化碘(ICl3),由于它们的性质与卤素相似,因此被称为卤素互化物。
(1)氯元素在元素周期表中的位置是____________________;ICl的电子式为____________。
(2)ICl与冷的NaOH稀溶液反应的离子方程式为________________________________。
(3)用海带制碘时,生成的粗碘中常混有ICl,可加入KI加热升华提纯,发生反应的化学方程式为_____。
(4)三氯化碘常以二聚体I2Cl6的形式存在,经电导仪测定知,它能发生部分电离,生成的两种离子的相对质量分别为198和269,其电离方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源:2015届广东省东莞市高三第一次调研考试理科化学试卷(解析版) 题型:填空题
(16分) 碳及其化合物有广泛的用途。
(1)反应C(s)+ H2O(g)  CO(g) +H2(g) ΔH= +131.3 kJ?mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
CO(g) +H2(g) ΔH= +131.3 kJ?mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是 。
A.增加碳的用量 B.升高温度 C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+ CO2(g) 2CO(g) △H=+172.5kJ?mol-1
2CO(g) △H=+172.5kJ?mol-1
则反应 CO(g)+H2O(g) CO2(g)+H2(g) 的△H= kJ?mol-1。
CO2(g)+H2(g) 的△H= kJ?mol-1。
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用稀硫酸作电解质溶液,多孔石墨做电极,该电池负极反应式为 。
(4)在一定温度下,将CO(g)和H2O(g)各0.16 mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下数据:
CO2(g)+H2(g),得到如下数据:
t / min | 2 | 4 | 7 | 9 |
n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
①其它条件不变,降低温度,达到新平衡前v(逆)_____v(正)(填“>”、“<”或“=”) 。
②该温度下,此反应的平衡常数K=__________;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),平衡时CO的体积分数______(填“增大”、“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源:2015届广东省东莞市高三第一次调研考试理科化学试卷(解析版) 题型:选择题
下列实验中,所加固体可以完全溶解的是
A.在H2O2溶液中加入少量MnO2粉末 B.将一小块铝片投入足量NaOH溶液中
C.将少量氢氧化铝加入足量的浓氨水中 D.常温下将一小块铁片投入足量的浓硝酸中
查看答案和解析>>
科目:高中化学 来源:2015届广东省七校高三上学期第一次联考理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.氨的催化氧化是一种特殊的固氮方式
B.工业冶炼铝:电解熔融AlCl3固体
C.将铁粉加入FeCl3、CuCl2混合溶液中,充分反应后剩余的固体中不一定有铁
D.用加热分解的方法可将NH4Cl固体和Ca(OH)2固体的混合物分离
查看答案和解析>>
科目:高中化学 来源:2015届山西省高三上学期期中考试化学试卷(解析版) 题型:实验题
(15分)氮化铝(AlN)是一种新型无机非金属材料。某AlN样品仅含有A12O3杂质,为测定AlN的含量,设计如下三种实验方案。(已知:A1N+NaOH+H2O=NaAlO2+NH3↑)
【方案l】取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。
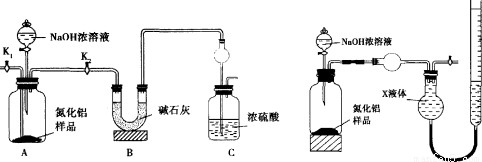
(1)左装置图中球形干燥管的作用是 。
(2)完成以下实验步骤:组装好实验装置,首先 ,再加入实验药品。接下来的实验操作是 ,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化。通入氮气的目的是 。
(3)由于装置存在缺陷,导致测定结果偏高。请提出改进意见 。
【方案2】用右上装置图测定mg样品中AlN的纯度(部分夹持装置已略去)。
(4)为测定生成气体的体积,量气装置中的X液体可以是 。
a.CCl4 b.H2O c.NH4Cl溶液 d.
(5)若m g样品完全反应,测得生成气体的体积为VmL(已转换为标准状况)。则AlN的质量分数是 。
【方案3】按下图步骤测定样品中A1N的纯度:
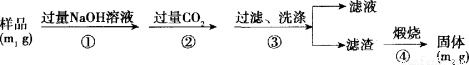
(6)步骤②生成沉淀的离子方程式为 。
(7)若在步骤③中未洗涤,测定结果将 (_填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源:2015届山西省高三上学期期中考试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.SO2、SiO2、NO2均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.“玉兔”月球车太阳能电池帆板的材料是二氧化硅
D.常温下pH=4的NaHC2O4溶液中:c(H2C2O4)<c(C2O42-)
查看答案和解析>>
科目:高中化学 来源:2015届山东省邹城市高三10月月考化学试卷(解析版) 题型:选择题
某无色溶液能与铝反应放出氢气,则该溶液中肯定不能大量共存的离子组是 ( )
A.NH4+、Na+、Ba2+、Cl- B.Na+、I-、HCO3-、SO42-
C.K+、Cl-、SO32-、AlO2- D.Na+、Mg2+、SO42-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com