
”¾ĢāÄæ”湤Ņµ²ÉÓĆĀČ»Æļ§±ŗÉÕĮāĆĢæóÖʱøøß“æĢ¼ĖįĆĢµÄĮ÷³ĢČēĶ¼ĖłŹ¾£ŗ

ŅŃÖŖ£ŗ¢ŁĮāĆĢæóµÄÖ÷ŅŖ³É·ÖŹĒMnCO3£¬ĘäÖŠŗ¬Fe”¢Ca”¢Mg”¢AlµČŌŖĖŲ”£
¢ŚAl3£«”¢Fe3£«³ĮµķĶźČ«µÄpH·Ö±šĪŖ4.7”¢3.2£¬Mn2£«”¢Mg2£«æŖŹ¼³ĮµķµÄpH·Ö±šĪŖ8.1”¢9.1”£
¢Ū±ŗÉÕ¹ż³ĢÖŠÖ÷ŅŖ·“Ó¦ĪŖMnCO3£«2NH4Cl ![]() MnCl2£«2NH3”ü£«CO2”ü£«H2O”£
MnCl2£«2NH3”ü£«CO2”ü£«H2O”£
(1)½įŗĻĶ¼1”¢2”¢3£¬·ÖĪö±ŗÉÕ¹ż³ĢÖŠ×ī¼ŃµÄ±ŗÉÕĪĀ¶Č”¢±ŗÉÕŹ±¼ä”¢m(NH4Cl)/m(ĮāĆĢæó·Ū)·Ö±šĪŖ____________”¢____________”¢____________”£

(2)¶Ō½ž³öŅŗ¾»»Æ³żŌÓŹ±£¬ŠčĻČ¼ÓČėMnO2½«Fe2£«×Ŗ»ÆĪŖFe3£«£¬ŌŁµ÷½ŚČÜŅŗpHµÄ·¶Ī§__£¬½«Fe3£«ŗĶAl3£«±äĪŖ³Įµķ¶ų³żČ„£¬Č»ŗó¼ÓČėNH4F½«Ca2£«”¢Mg2£«±äĪŖ·ś»ÆĪļ³Įµķ³żČ„”£
(3)”°Ģ¼»Æ½į¾§”±²½ÖčÖŠ£¬¼ÓČėĢ¼ĖįĒāļ§Ź±·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ____”£
(4)ÉĻŹöĮ÷³ĢÖŠæÉŃ»·Ź¹ÓƵÄĪļÖŹŹĒ________”£
(5)ĻÖÓƵĪ¶Ø·Ø²ā¶Ø½ž³öŅŗÖŠMn2£«µÄŗ¬Į攣ŹµŃé²½Öč£ŗ³ĘČ”1.000 gŹŌŃł£¬ĻņĘäÖŠ¼ÓČėÉŌ¹żĮæµÄĮ×ĖįŗĶĻõĖį£¬¼ÓČČŹ¹·“Ó¦2Mn2£«£«NO3-£«4PO43-£«2H£«![]() 2[Mn(PO4)2]3££«NO2-£«H2O³ä·Ö½ųŠŠ²¢³żČ„¶ąÓąµÄĻõĖį£»¼ÓČėÉŌ¹żĮæµÄĮņĖįļ§£¬·¢Éś·“Ó¦NO2-£«NH4+===N2”ü£«2H2OŅŌ³żČ„NO2-£»¼ÓČėĻ”ĮņĖįĖį»Æ£¬ÓĆ2.00 mol”¤L£110.00 mLĮņĖįŃĒĢśļ§±ź×¼ČÜŅŗ½ųŠŠµĪ¶Ø£¬·¢ÉśµÄ·“Ó¦ĪŖ[Mn(PO4)2]3££«Fe2£«===Mn2£«£«Fe3£«£«2PO43-£»ÓĆ0.10 mol”¤L£110.00 mLĖįŠŌK2Cr2O7ČÜŅŗĒ”ŗĆ³żČ„¹żĮæµÄFe2£«”£
2[Mn(PO4)2]3££«NO2-£«H2O³ä·Ö½ųŠŠ²¢³żČ„¶ąÓąµÄĻõĖį£»¼ÓČėÉŌ¹żĮæµÄĮņĖįļ§£¬·¢Éś·“Ó¦NO2-£«NH4+===N2”ü£«2H2OŅŌ³żČ„NO2-£»¼ÓČėĻ”ĮņĖįĖį»Æ£¬ÓĆ2.00 mol”¤L£110.00 mLĮņĖįŃĒĢśļ§±ź×¼ČÜŅŗ½ųŠŠµĪ¶Ø£¬·¢ÉśµÄ·“Ó¦ĪŖ[Mn(PO4)2]3££«Fe2£«===Mn2£«£«Fe3£«£«2PO43-£»ÓĆ0.10 mol”¤L£110.00 mLĖįŠŌK2Cr2O7ČÜŅŗĒ”ŗĆ³żČ„¹żĮæµÄFe2£«”£
¢ŁĖįŠŌK2Cr2O7ČÜŅŗÓėFe2£«·“Ó¦(»¹Ō²śĪļŹĒCr3£«)µÄĄė×Ó·½³ĢŹ½ĪŖ___________”£
¢ŚŹŌŃłÖŠĆĢµÄÖŹĮæ·ÖŹżĪŖ________”£
”¾“š°ø”æ500 ”ę 60 min 1.10 4.7”ÜpH<8.1 Mn2£«£«2HCO3-===MnCO3”ż£«CO2”ü£«H2O NH4Cl 6Fe2£«£«Cr2O72-£«14H£«===6Fe3£«£«2Cr3£«£«7H2O 77%
”¾½āĪö”æ
(1)øł¾ŻĶ¼Ļń·ÖĪö£¬±ŗÉÕĪĀ¶ČŌŚ500 ”ęŅŌÉĻ”¢±ŗÉÕŹ±¼äŌŚ60 minŅŌÉĻ”¢![]() ŌŚ1.1ŅŌÉĻ£¬ĆĢ½ž³öĀŹ³¬¹ż90% £»
ŌŚ1.1ŅŌÉĻ£¬ĆĢ½ž³öĀŹ³¬¹ż90% £»
(2)¾»»Æ³żŌÓµÄÄæµÄŹĒ½«Fe3£«ŗĶAl3£«±äĪŖ³Įµķ³żČ„£¬²¢ĒŅ±£Ö¤Mn2£«²»ÄܳĮµķ£»
(3)”°Ģ¼»Æ½į¾§”±²½ÖčÖŠ£¬Ģ¼ĖįĒāļ§ÓėĆĢĄė×Ó·“Ӧɜ³ÉĢ¼ĖįĆĢ³ĮµķŗĶ¶žŃõ»ÆĢ¼ĘųĢ壻
(4)øł¾ŻĮ÷³ĢĶ¼·ÖĪöæÉŃ»·Ź¹ÓƵÄĪļÖŹ£»
(5) ¢Łøł¾ŻµĆŹ§µē×ÓŹŲŗćŹéŠ“ĖįŠŌK2Cr2O7ČÜŅŗÓėFe2£«·“Ó¦µÄĄė×Ó·½³ĢŹ½£»
¢Śøł¾Ż¹ŲĻµŹ½Mn2£«”«[Mn(PO4)2]3£”«Fe2£«¼ĘĖćĆĢµÄÖŹĮæ·ÖŹż£»
(1)øł¾ŻĶ¼Ļń·ÖĪö£¬±ŗÉÕĪĀ¶ČŌŚ500 ”ęŅŌÉĻ”¢±ŗÉÕŹ±¼äŌŚ60 minŅŌÉĻ”¢![]() ŌŚ1.1ŅŌÉĻ£¬ĆĢ½ž³öĀŹ³¬¹ż90% £¬ĖłŅŌ±ŗÉÕ¹ż³ĢÖŠ×ī¼ŃµÄ±ŗÉÕĪĀ¶Č”¢±ŗÉÕŹ±¼ä”¢
ŌŚ1.1ŅŌÉĻ£¬ĆĢ½ž³öĀŹ³¬¹ż90% £¬ĖłŅŌ±ŗÉÕ¹ż³ĢÖŠ×ī¼ŃµÄ±ŗÉÕĪĀ¶Č”¢±ŗÉÕŹ±¼ä”¢![]() ·Ö±šĪŖ500 ”ę”¢60 min”¢ 1.10£»
·Ö±šĪŖ500 ”ę”¢60 min”¢ 1.10£»
(2)¾»»Æ³żŌÓµÄÄæµÄŹĒ½«Fe3£«ŗĶAl3£«±äĪŖ³Įµķ³żČ„£¬²¢ĒŅ±£Ö¤Mn2£«²»ÄܳĮµķ£¬ĖłŅŌµ÷½ŚČÜŅŗpHµÄ·¶Ī§ĪŖ4.7”ÜpH<8.1£»
(3)”°Ģ¼»Æ½į¾§”±²½ÖčÖŠ£¬Ģ¼ĖįĒāļ§ÓėĆĢĄė×Ó·“Ӧɜ³ÉĢ¼ĖįĆĢ³ĮµķŗĶ¶žŃõ»ÆĢ¼ĘųĢ壬·“Ó¦Ąė×Ó·½³ĢŹ½ŹĒMn2£«£«2HCO3-===MnCO3”ż£«CO2”ü£«H2O£»
(4)øł¾ŻĮ÷³ĢĶ¼£¬æÉŃ»·Ź¹ÓƵÄĪļÖŹŹĒNH4Cl£»
(5) ¢Łøł¾ŻµĆŹ§µē×ÓŹŲŗć£¬ĖįŠŌK2Cr2O7ČÜŅŗÓėFe2£«·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ6Fe2£«£«Cr2O72-£«14H£«===6Fe3£«£«2Cr3£«£«7H2O£»
¢ŚCr2O72-µÄĪļÖŹµÄĮæŹĒ0.10 mol”¤L£1”Į0.01L=0.001mol£¬·“Ó¦6Fe2£«£«Cr2O72-£«14H£«===6Fe3£«£«2Cr3£«£«7H2OĻūŗÄFe2£«µÄĪļÖŹµÄĮæŹĒ0.006mol£¬ [Mn(PO4)2]3££«Fe2£«===Mn2£«£«Fe3£«£«2PO43-ĻūŗÄFe2£«µÄĪļÖŹµÄĮæŹĒ2.00 mol”¤L£1”Į0.01L£0.006mol=0.014mol£¬øł¾ŻMn2£«”«[Mn(PO4)2]3£”«Fe2£«£¬æÉÖŖMn2£«µÄĪļÖŹµÄĮæŹĒ0.014mol£¬ĆĢµÄÖŹĮæ·ÖŹżĪŖ![]() ”£
ӣ


 »ĘøŌŠ”דŌŖ½ā¾öĪŹĢāĢģĢģĮ·ĻµĮŠ“š°ø
»ĘøŌŠ”דŌŖ½ā¾öĪŹĢāĢģĢģĮ·ĻµĮŠ“š°ø ČżµćŅ»²āæģĄÖÖÜ¼Ę»®ĻµĮŠ“š°ø
ČżµćŅ»²āæģĄÖÖÜ¼Ę»®ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪųŹĒŅ»ÖÖ·Ē½šŹō£¬æÉŅŌÓĆ×÷¹āĆō²ÄĮĻ”¢µē½āĆĢŠŠŅµ“߻ƼĮ£®
£Øl£©SeŹĒŌŖĖŲÖÜĘŚ±ķÖŠµŚ34ŗÅŌŖĖŲ£¬Ę仳Ģ¬Ō×ÓµÄŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ__£®
£Ø2£©øł¾Ż¼Ū²ćµē×Ó¶Ō»„³āĄķĀŪ£¬æÉŅŌĶĘÖŖSeO3µÄ·Ö×Óæռ乹ŠĶĪŖ__£¬ĘäÖŠSeŌ×Ó²ÉÓĆµÄ¹ģµĄŌӻƊĪŹ½ĪŖ__”£
£Ø3£©CSe2ÓėCO2½į¹¹ĻąĖĘ£¬CSe2·Ö×ÓÄŚ¦Ņ¼üÓė¦Š¼üøöŹżÖ®±ČĪŖ__£¬CSe2Ź×“ĪŹĒÓÉH2SeÓėCCl4·“Ó¦ŗóÖĘČ”µÄ£¬CSe2·Ö×ÓÄŚµÄSe©C©Se¼ü½Ē__£ØĢī”°“óÓŚ”±£¬”°µČÓŚ”±»ņ”°Š”ÓŚ”±£©H2Se·Ö×ÓÄŚµÄH©Se©H¼ü½Ē”£
£Ø4£©Īų»Æļؾ§ĢåŹōÓŚ·“Ó©ŹÆŠĶ½į¹¹£¬¾§°ū½į¹¹ČēĶ¼ĖłŹ¾”£Ćæøö¾§°ūÖŠ°üŗ¬__øöRb2Seµ„ŌŖ£¬ĘäÖŠSe2©ÖÜĪ§ÓėĖü¾ąĄė×ī½üĒŅĻąµČµÄRb+µÄĄė×ÓŹżÄæĪŖ__”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°±ŹĒ»ÆѧŹµŃéŹŅ¼°»Æ¹¤Éś²śÖŠµÄÖŲŅŖĪļÖŹ£¬Ó¦ÓĆ¹ć·ŗ”£N2(g)£«3H2(g)![]() 2NH3(g) ¦¤H=-92.2kJ/mol
2NH3(g) ¦¤H=-92.2kJ/mol
£Ø1£©ŌŚŗćĪĀŗćČŻĆܱÕČŻĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬ĘšŹ¼Ķ¶ĮĻŹ±ø÷ĪļÖŹÅضČČēĻĀ±ķ£ŗ
N2 | H2 | NH3 | |
Ķ¶ĮĻ¢ń | 1.0 mol/L | 3.0 mol /L | 0 |
Ķ¶ĮĻ¢ņ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
¢Ł°“Ķ¶ĮĻ¢ń½ųŠŠ·“Ó¦£¬²āµĆ“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±H2µÄ×Ŗ»ÆĀŹĪŖ40%£¬ŌņøĆĪĀ¶ČĻĀŗĻ³É°±·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ_____________”£
¢Ś°“Ķ¶ĮĻ¢ņ½ųŠŠ·“Ó¦£¬ĘšŹ¼Ź±·“Ó¦½ųŠŠµÄ·½ĻņĪŖ________£ØĢī”°ÕżĻņ”±»ņ”°ÄęĻņ”±£©”£
¢ŪČōÉżøßĪĀ¶Č£¬ŌņŗĻ³É°±·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż________£ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©”£
£Ø2£©L£ØL1”¢L2£©”¢XæÉ·Ö±š“ś±ķŃ¹Ēæ»ņĪĀ¶Č”£ĻĀĶ¼±ķŹ¾LŅ»¶ØŹ±£¬ŗĻ³É°±·“Ó¦ÖŠH2(g)µÄĘ½ŗā×Ŗ»ÆĀŹĖęXµÄ±ä»Æ¹ŲĻµ”£

¢” X“ś±ķµÄĪļĄķĮæŹĒ______”£
¢¢ ÅŠ¶ĻL1”¢L2µÄ“󊔹ŲĻµ£¬²¢¼ņŹöĄķÓÉ£ŗ______”£
£Ø3£©µē»ÆѧĘųĆō“«øŠĘ÷æÉÓĆÓŚ¼ą²ā»·¾³ÖŠNH3µÄŗ¬Į棬Ę乤×÷ŌĄķŹ¾ŅāĶ¼ČēĻĀ£ŗ

¢Ł µē¼«bÉĻ·¢ÉśµÄŹĒ______·“Ó¦£ØĢī”°Ńõ»Æ”±»ņ”°»¹Ō”±£©
¢Ś Š“³öµē¼«aµÄµē¼«·“Ó¦Ź½£ŗ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹śæĘѧ¼ŅŌŚĢģČ»ĘųĶŃĮņŃŠ¾æ·½ĆęČ”µĆĮĖŠĀ½ųÕ¹£¬ĄūÓĆČēĶ¼×°ÖĆæÉ·¢Éś·“Ó¦£ŗH2S+O2=H2O2+S£¬ŅŃÖŖ¼×³ŲÖŠ·¢ÉśµÄ·“Ó¦£ŗ


ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ¼×³ŲÖŠĢ¼°ōÉĻ·¢ÉśµÄµē¼«·“Ó¦ĪŖAQ+2H+-2e-=H2AQ
B. ŅŅ³ŲČÜŅŗÖŠ·¢ÉśµÄ·“Ó¦ĪŖH2S+I3-=3I-+S+2H+
C. øĆ×°ÖĆÖŠµēÄÜ×Ŗ»ÆĪŖ¹āÄÜ
D. H+“Ӽ׳ŲŅĘĻņŅŅ³Ų
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°±ŹĒ»ÆѧŹµŃéŹŅ¼°»Æ¹¤Éś²śÖŠµÄÖŲŅŖĪļÖŹ£¬Ó¦ÓĆ¹ć·ŗ”£N2(g)£«3H2(g)![]() 2NH3(g) ¦¤H=-92.2kJ/mol
2NH3(g) ¦¤H=-92.2kJ/mol
£Ø1£©ŌŚŗćĪĀŗćČŻĆܱÕČŻĘ÷ÖŠ½ųŠŠŗĻ³É°±·“Ó¦£¬ĘšŹ¼Ķ¶ĮĻŹ±ø÷ĪļÖŹÅضČČēĻĀ±ķ£ŗ
N2 | H2 | NH3 | |
Ķ¶ĮĻ¢ń | 1.0 mol/L | 3.0 mol /L | 0 |
Ķ¶ĮĻ¢ņ | 0.5 mol/L | 1.5 mol/L | 1.0 mol/L |
¢Ł°“Ķ¶ĮĻ¢ń½ųŠŠ·“Ó¦£¬²āµĆ“ļµ½»ÆŃ§Ę½ŗāדĢ¬Ź±H2µÄ×Ŗ»ÆĀŹĪŖ40%£¬ŌņøĆĪĀ¶ČĻĀŗĻ³É°±·“Ó¦µÄĘ½ŗā³£Źż±ķ“ļŹ½ĪŖ_____________”£
¢Ś°“Ķ¶ĮĻ¢ņ½ųŠŠ·“Ó¦£¬ĘšŹ¼Ź±·“Ó¦½ųŠŠµÄ·½ĻņĪŖ________£ØĢī”°ÕżĻņ”±»ņ”°ÄęĻņ”±£©”£
¢ŪČōÉżøßĪĀ¶Č£¬ŌņŗĻ³É°±·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż________£ØĢī”°±ä“ó”±”¢”°±äŠ””±»ņ”°²»±ä”±£©”£
£Ø2£©L£ØL1”¢L2£©”¢XæÉ·Ö±š“ś±ķŃ¹Ēæ»ņĪĀ¶Č”£ĻĀĶ¼±ķŹ¾LŅ»¶ØŹ±£¬ŗĻ³É°±·“Ó¦ÖŠH2(g)µÄĘ½ŗā×Ŗ»ÆĀŹĖęXµÄ±ä»Æ¹ŲĻµ”£

¢” X“ś±ķµÄĪļĄķĮæŹĒ______”£
¢¢ ÅŠ¶ĻL1”¢L2µÄ“󊔹ŲĻµ£¬²¢¼ņŹöĄķÓÉ£ŗ______”£
£Ø3£©µē»ÆѧĘųĆō“«øŠĘ÷æÉÓĆÓŚ¼ą²ā»·¾³ÖŠNH3µÄŗ¬Į棬Ę乤×÷ŌĄķŹ¾ŅāĶ¼ČēĻĀ£ŗ
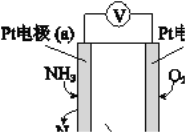
¢Ł µē¼«bÉĻ·¢ÉśµÄŹĒ______·“Ó¦£ØĢī”°Ńõ»Æ”±»ņ”°»¹Ō”±£©
¢Ś Š“³öµē¼«aµÄµē¼«·“Ó¦Ź½£ŗ_________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A. 17g H2O2ÖŠŗ¬ÓŠ·Ē¼«ŠŌ¼üµÄŹżÄæĪŖNA
B. ³£ĪĀ³£Ń¹ĻĀ£¬17g¼×»ł£Ø-14CH3£©Ėłŗ¬µÄÖŠ×ÓŹżĪŖ9NA
C. ŌŚŗ¬CO32-×ÜŹżĪŖNAµÄNa2CO3ČÜŅŗÖŠ£¬Na+×ÜŹżĪŖ2NA
D. 13. 8g NO2Óė×ćĮæĖ®·“Ó¦£¬×ŖŅʵĵē×ÓŹżĪŖ0.2NA
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æW”¢X”¢Y”¢ZĖÄÖÖŌŖĖŲ·Ö±šŹĒŌŖĖŲÖÜĘŚ±ķÖŠĮ¬ŠųČżøö¶ĢÖÜĘŚµÄŌŖĖŲ£¬ĒŅŌ×ÓŠņŹżŅĄ“ĪŌö“󔣻ÆŗĻĪļXW3ÄÜ×÷ÖĘĄä¼ĮĒŅĘäÅØČÜŅŗæɼģŃéZµ„ÖŹŹĒ·ńŠ¹Ā¶£¬»ÆŗĻĪļYZ3ÄÜ“Ł½ųĖ®µÄµēĄė£¬ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A. ¼ņµ„Ąė×Ó°ė¾¶£ŗr(Z)>r(X)>r(Y)B. YµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĪŖĒæ¼ī
C. X2W4·Ö×ÓÖŠ¼Čŗ¬¼«ŠŌ¼ü£¬ÓÖŗ¬·Ē¼«ŠŌ¼üD. »ÆŗĻĪļXW3µÄĖ®ČÜŅŗÄÜŅÖÖĘĖ®µÄµēĄė
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷ÄÜ“ļµ½ÄæµÄŹĒ
A. ÓĆPHŹŌÖ½²ā¶Ø“ĪĀČĖįČÜŅŗµÄpH
B. ½«FeCl3ČÜŅŗ¼ÓČČÕōøɲ¢×ĘÉÕ»ńµĆFe2O3¹ĢĢå
C. ĻņĆ÷·ÆČÜŅŗÖŠ¼ÓČėŅ»¶ØĮæNaOH£¬ÖʱøAl(OH)3½ŗĢå
D. ŹŅĪĀĻĀ£¬²āµĆpH=5µÄNaHSO4ČÜŅŗÓėpH=9µÄNaHCO3ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąµČ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. 0.1 mol±ūĻ©ĖįÖŠŗ¬ÓŠµÄĖ«¼üŹżÄæĪŖ0.1 NA
B. ±ź×¼×“æöĻĀ£¬2.24LH2OÖŠŗ¬ÓŠµÄ¹²¼Ū¼üŹżÄæĪŖ0.2NA
C. 6.2 g°×Į×·Ö×ÓÖŠŗ¬P”ŖP¼üĪŖ0.2 NA
D. 7.8 g Na2O2ŗĶNa2SµÄ¹ĢĢå»ģŗĻĪļÖŠŗ¬ÓŠµÄĄė×Ó×ÜŹżĪŖ0.3 NA
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com