
| A. | 0.8 mol/LAg+ | B. | 0.4mol/L Ba2+ | C. | 0.4mol/L Mg2+ | D. | 0.2mol/L CO32- |
分析 0.4mol/LCl-、0.8mol/L SO42-、0.2mol/LAl3+、0.6mol/LH+、R离子,由电荷守恒可知0.4+0.8×2>0.2×3+0.6,则R为阳离子,结合离子共存来解答.
解答 解:由电荷守恒可知0.4+0.8×2>0.2×3+0.6,则R为阳离子,
R不能为Ag+,与Cl-、SO42-不能共存;
R不能为Ba2+,与SO42-不能共存,
则R只能为Mg2+,其浓度为$\frac{0.4+0.8×2-0.2×3+0.6}{2}$=0.4mol/L,
故选C.
点评 本题考查物质的量浓度的计算,为高频考点,把握电荷守恒及离子共存为解答的关键,侧重分析与计算能力的考查,注意电荷守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 锅炉水垢中的硫酸钙可用碳酸钠溶液处理,使之转化为碳酸钙,再用盐酸除去 | |
| B. | 铝制品不能存放酸性食物,但可长期存放咸的食物 | |
| C. | 铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝 | |
| D. | 海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
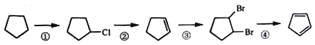
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一个原子轨道就是电子在原子核外的一个空间运动状态 | |
| B. | 电子云表示处于一定空间运动状态电子在核外空间的概率密度分布的描述 | |
| C. | 原子轨道伸展方向与能量大小是无关的 | |
| D. | 除s电子云外,其他空间运动状态的电子云也可以是球形的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | Mg2+ | C. | Cl- | D. | NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后容器内的气体只有CO | |
| B. | 反应后生成的CO与反应前的CO2的物质的量之比为1:1 | |
| C. | 反应后生成的CO与反应前的CO2的分子数目之比为3:2 | |
| D. | 反应后容器内的气体与反应前的CO2所含的氧原子数目之比为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶于水后能形成无色溶液的红棕色气体一定是Br2 | |
| B. | 能使润湿的淀粉碘化钾试纸变蓝的气体一定是Cl2 | |
| C. | 遇空气立即形成红棕色气体的一定是NO | |
| D. | 在潮湿空气中能形成白雾的气体一定是HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 肯定含有碳、氢、氧三种元素 | |
| B. | 肯定含有碳、氢元素,可能含有氧元素 | |
| C. | 肯定含有碳、氢元素,不含氧元素 | |
| D. | 该有机物是甲醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com