
| A. | 3S+6NaOH═Na2SO3+2Na2S+3H2O | |
| B. | 3NO2+H2O═2HNO3+NO | |
| C. | 2FeCl2+Cl2=3FeCl3 | |
| D. | 4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O |
分析 A.3S+6NaOH═Na2SO3+2Na2S+3H2O中,2molS作氧化剂与1molS作还原剂时转移电子相等;
B.3NO2+H2O═2HNO3+NO中,1molNO2作氧化剂与2molNO2作还原剂时转移电子相等;
C.Cl元素的化合价降低,Fe元素的化合价升高,Cl2为氧化剂,FeCl2为还原剂;
D.Mn元素的化合价降低,Cl元素的化合价升高,则1molMnO2与2molHCl转移电子相等.
解答 解:A.3S+6NaOH═Na2SO3+2Na2S+3H2O中,2molS作氧化剂与1molS作还原剂时转移电子相等,则氧化剂与还原剂物质的量的比2:1,故A选;
B.3NO2+H2O═2HNO3+NO中,1molNO2作氧化剂与2molNO2作还原剂时转移电子相等,则氧化剂与还原剂物质的量的关系是1:2,故B不选;
C.Cl元素的化合价降低,Fe元素的化合价升高,Cl2为氧化剂,FeCl2为还原剂,则氧化剂与还原剂物质的量的关系是1:2,故C不选;
D.Mn元素的化合价降低,Cl元素的化合价升高,则1molMnO2与2molHCl转移电子相等,则氧化剂与还原剂物质的量的关系是1:2,故D不选;
故选A.
点评 本题考查氧化还原反应及计算,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子转移守恒,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 0.2mol/L | B. | 0.4 mol/L | C. | 0.8mol/L | D. | 0.7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
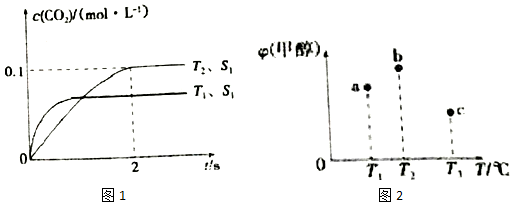
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 0.4 | 0.6 | 1.0 | 1.1 | 1.7 |
| 时间(min) | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强比(p后/p前) | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体通过盛有水的洗气瓶 | |
| B. | 通过装有过量浓溴水的洗气瓶 | |
| C. | 先将混合气体通过酸性高锰酸钾溶液中,然后再通入NaOH溶液中 | |
| D. | 混合气与过量氢气混合 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 34S2-的结构示意图: | B. | H2O2的电子式: | ||
| C. | 甲烷分子的比例模型: | D. | 中子数为18的硫原子:${\;}_{16}^{18}$S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
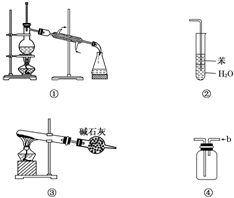
| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,能够防止倒吸 | |
| C. | 以NH4HCO3为原料,装置③可用于制备少量CO2 | |
| D. | 装置④a口进气可收集Cl2、NO2等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑥ | B. | ①③④ | C. | ①③⑤⑥ | D. | ②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com