
【题目】高铁电池是一种新型可充电电池该电池能较长时间保持稳定的放电电压。高铁电池的总反应为3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
(1)高铁电池的负极材料是______________。
(2)放电时,正极发生______________(填“氧化”或“还原”)反应;正极的电极反应式为______________。
科目:高中化学 来源: 题型:
【题目】有机物A是合成二氢荆芥内酯的重要原料,其结构简式如下图,下列检验A中官能团的试剂和顺序正确的是( )
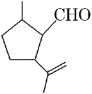
A. 先加酸性高锰酸钾溶液,后加银氨溶液,微热
B. 先加溴水,后加酸性高锰酸钾溶液
C. 先加银氨溶液,微热,再加入溴水
D. 先加入新制氢氧化铜,微热,酸化后再加溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用莤烯(A)为原料可制得杀虫剂菊酯(H),其合成路线可表示如下:
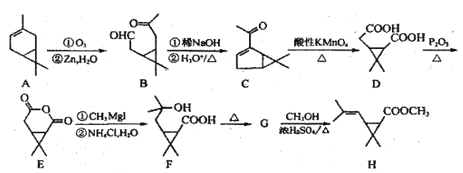
已知:R1CHO+R2CH2CHO
(1)写出一分子的 F 通过酯化反应生成环酯的结构简式__________。
(2)写出 G 到 H 反应的化学方程式___________。
(3)写出满足下列条件的 C 的一种同分异构体的结构简式______________。
①能与FeCl3 溶液发生显色反应;②分子中有 4 种不同化学环境的氢。
(4)写出以![]() 和 CH3CH2OH为原料制备
和 CH3CH2OH为原料制备![]() 的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩,如图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是
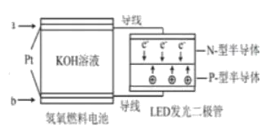
A.通入O2的电极发生反应:O2+4e-=2O2-
B.a处通入氧气,b处通氢气
C.电池放电后,OH-的物质的量浓度减小
D.电路中的电子从负极经外电路到正极,再经过KOH溶液回到负极,形成闭合回路
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环氧树脂因其具有良好的机械性能、绝缘性能以及与各种材料的粘结性能,已广泛应用于涂料和胶黏剂等领域。下面是制备一种新型环氧树脂G的合成路线:
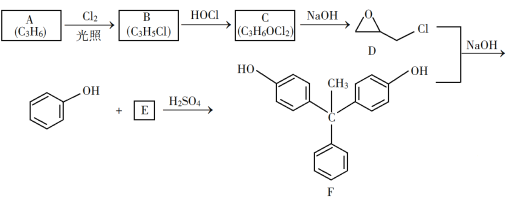
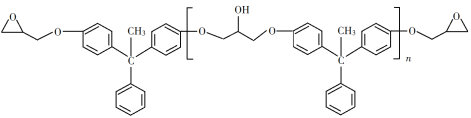
已知以下信息:
①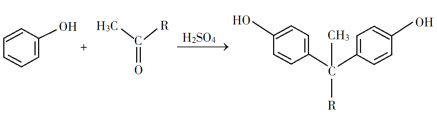 +H2O
+H2O
②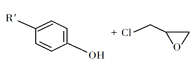 +NaOH
+NaOH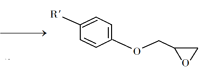 +NaCl+H2O
+NaCl+H2O
③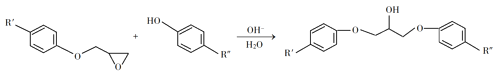
回答下列问题:
(1)A是一种烯烃,化学名称为_____,C中官能团的名称为_____、____。
(2)由C生成D反应方程式为_______。
(3)由B生成C的反应类型为_______。
(4)E的结构简式为_______。
(5)E的二氯代物有多种同分异构体,请写出其中能同时满足以下条件的芳香化合物的结构简式________、_______。
①能发生银镜反应;②核磁共振氢谱有三组峰,且峰面积比为3∶2∶1。
(6)假设化合物D、F和NaOH恰好完全反应生成1 mol单一聚合度的G,若生成的NaCl和H2O的总质量为765g,则G的n值理论上应等于_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以工业级氧化锌(含Fe2+、Mn2+、Cu2+、Ni2+等)为原料制备氧化锌的流程如下:
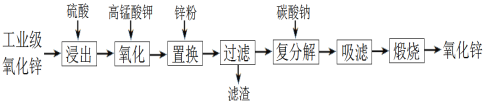
其中“氧化”加入KMnO4是为了除去浸出液中的Fe2+和Mn2+。下列有关说法错误的是
A. 浸出时通过粉碎氧化锌提高了浸出率
B. “氧化”生成的固体是MnO2和Fe(OH)3
C. “置换”加入锌粉是为了除去溶液中的Cu2+、Ni2+等
D. “煅烧”操作用到的仪器:玻璃棒、蒸发皿、泥三角
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为某有机物与各种试剂的反应现象,则这种有机物可能是( )
试剂 | 钠 | 溴水 |
|
现象 | 放出气体 | 褪色 | 放出气体 |
A.CH2=CH-CH2-OHB.![]()
C.CH2=CH-COOHD.CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列各溶液中有关微粒的物质的量浓度关系正确的是( )
A. 0.1 mol·L-1 NaHCO3溶液:c(OH-)=c(H+)+c(HCO3-)+c(H2CO3)-c(CO32-)
B. 0.1 mol·L-1 NaHC2O4溶液呈酸性:c(Na+)>c(HC2O4-)>c(H2C2O4)>c(C2O42-)
C. 20 mL 0.10 mol·L-1 CH3COONa溶液与10 mL 0.10 mol·L-1 HCl溶液混合得到的酸性溶液:c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-)
D. 向0.1mol·L-1 NH4HSO4溶液中滴加NaOH溶液至恰好呈中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,某恒容密闭容器中含有NO2、N2O4两种气体,反应开始至达到平衡状态过程中,两种物质的浓度随时间的变化如下所示。

(1)表示NO2浓度变化的曲线是_____,写出相应的化学方程式:____________________。
(2)从反应开始至达到平衡的过程中,用N2O4表示的反应速率v(N2O4)=_____,a、b两点对应状态中,曲线X代表的物质的反应速率相对大小为v(a)_____v(b)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com