
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则
| A.原子半径:丙<丁<乙 | B.乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| C.甲、乙、丙的氧化物均为共价化合物 | D.单质的还原性:丁>丙>甲 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:单选题
随着卤素原子半径的增大,下列递变规律正确的是
| A.单质熔、沸点逐渐降低 | B.气态氢化物稳定性逐渐增强 |
| C.卤素离子的还原性逐渐增强 | D.元素的非金属性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关原子结构或元素性质说法正确的是
| A.原子核外电子排布式为1s2的元素与原子核外电子排布式为1s22s2的元素化学性质相似 |
B.基态碳原子的价电子排布图: |
C.基态铜原子的价电子排布图: |
| D.Fe3+的最外层电子排布式为:3s23p63d5 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W四种短周期元素在周期表的位置如图,Y原子的最外层电子数是其次外层电子数的3倍,下列说法正确的是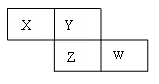
| A.气态氢化物的稳定性:X>Y |
| B.Z元素的氧化物对应的水化物一定是一种强酸 |
| C.X、Y、Z原子半径的大小顺序: X>Y>Z |
| D.X的气态氢化物与W的气态氢化物可以相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法正确的是
| A.第ⅦA族元素的非金属性比第ⅥA族元素的强 |
| B.第三周期元素的简单阳离子半径从左到右逐渐减小 |
| C.第ⅤA族元素非金属氧化物对应的水化物的酸性从上到下依次减弱 |
| D.依据元素周期表、周期律推测尚未发现的第七周期第ⅦA族元素应为非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
2012年,IUPAC正式命名了116号元素,但117号元素尚未被正式认定。下列关于 的说法,错误的是
的说法,错误的是
| A.是两种原子 | B.互为同位素 |
| C.中子数分别为176和177 | D.电子数相差1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期主族元素A、B、C、D的原子序数依次增大,A、C的原子序数的差是8,A原子的最外层电子数是其次外层电子数的3倍,在同周期主族元素中B原子的原子半径最大。下列说法正确的是
A.气态氢化物的热稳定性:A<C
B.元素A与B只能形成一种化合物
C.元素B与D形成的化合物是离子化合物
D.最高价氧化物对应的水化物的酸性:C>D
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
图表法、图象法是常用的科学研究方法。
(1)短周期某主族元素M的电离能情况如图A所示。则M元素位于周期表的第 族。
(2)图B是研究部分元素的氢化物的沸点变化规律的图像,折线c可以表达出第 族元素氢化物的沸点的变化规律。不同同学对某主族元素氢化物的沸点的变化趋势画出了两条折线——折线a和折线b,你认为正确的是: (填“a”或“b”)。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期金属元素甲~戊在元素周期表中的相对位置如表中所示。下列判断正确的是
| 甲 | 乙 | |
| 丙 | 丁 | 戊 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com