
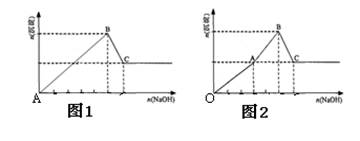
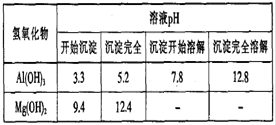
| A����ͼ�����n(Mg2+): n(Al3+)=2:1 |
| B��ͼ1ʵ���У�OA���������ֳ��� |
| C������������Ϣ�ó���Ӧ���¶��£�Ksp(Al(OH)3)> Ksp(Mg(OH)2) |
| D����ϱ������ݺ�ͼ2������AB�ο��ܷ�����Mg2++2AlO2��+4H2O ��2Al(OH)3��+Mg(OH)2�� |
 �����Ļ�������ҵϵ�д�
�����Ļ�������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����Һ�ļ���̫�� | B��Al3+���백ˮ��Ӧ |
| C�����ɵ�Al(OH)3�ܽ��� | D��Al3+��������F-��������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
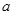 g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊ
g��Ʒ�������м���������NaOH��Һ��������ɵ����壨��״������ͬ�����Ϊ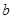 L����Ӧ�Ļ�ѧ����ʽ��_________________����Ʒ������������____________g��
L����Ӧ�Ļ�ѧ����ʽ��_________________����Ʒ������������____________g�� g��Ʒ�ڸ����½���ǡ����ȫ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�__________________����������������������____________��
g��Ʒ�ڸ����½���ǡ����ȫ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽ�ǣ�__________________����������������������____________�� L���������루1������������������
L���������루1������������������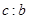 ��_________��
��_________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��200mL | B��250 mL | C��425mL | D��560mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NaOH | B��H2SO4 | C��NH3?H2O | D��KOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
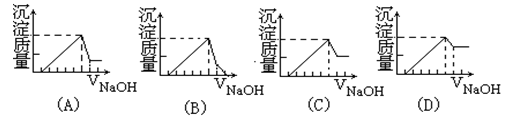
 Y��Һ�зֱ����NaOH��HClʱ�������������ʵ�����������������������Һ���֮��Ĺ�ϵ������˵����ȷ����(����)
Y��Һ�зֱ����NaOH��HClʱ�������������ʵ�����������������������Һ���֮��Ĺ�ϵ������˵����ȷ����(����)
| A��X��Һ����ΪAlCl3,Y��Һ����ΪNaAlO2 |
| B��b���߱�ʾ������X��Һ�м���NaOH��Һ |
| C����O��ʱ��������������ҺŨ����� |
| D��a��b���߱�ʾ�ķ�Ӧ����������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com