
室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如下图,下列有关说法正确的是
A.a点时,溶液呈酸性的原因是Al3+水解,离子方程式为:
Al3++3OH- Al(OH)3
Al(OH)3
B.a→b段,溶液pH增大,Al3+浓度不变
C.b→c段,加入的OH-主要用于生成Al(OH)3沉淀
D.d点时,Al(OH)3沉淀开始溶解

科目:高中化学 来源: 题型:
元素周期表中某区域的一些元素多用于制造半导体材料,它们是
A.碱土金属元素
B.元素周期表中第3~12列的过渡元素
C.金属元素和非金属元素分界线附近的元素
D.左下方区域的金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
有一无色溶液,其中可能含有Fe3+、Al3+、Fe2+、Mg2+、Cu2+、NH4+、K+、
CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其操作和有关现象如下图所示:





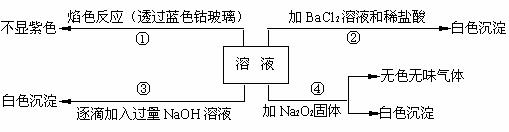
(1)在原溶液中一定不存在的离子有 ;
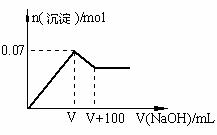
(2)第③个实验中,若取原溶液的体积为100 mL,
滴加的NaOH溶液的物质的量浓度为0.5 mol·L-1 且
生成白色沉淀的量与加入NaOH的量有右图所示的相
互关系,则该溶液中所含阳离子的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
用铝粉和氧化铁粉末配成的铝热剂,分成两等份:一份在高温下恰好完全反应,再与足量稀硫酸反应,生成氢气aL;另一份直接放入足量烧碱溶液中充分反应,在相同条件下生气氢气bL,则体积比a:b为
A.1:1 B.3:2 C.2:3 D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Fe2(SO4)3溶液的叙述正确的是
A、该溶液中K+、Fe2+、C6H5OH、Br-可以大量共存
B、和KI溶液反应的离子方程式:Fe3++2I- Fe2++I2
Fe2++I2
C、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42—+Ba2++3OH- Fe(OH)3+ Ba SO4
Fe(OH)3+ Ba SO4
D、1 L0.1 mol·L—1该溶液和足量的Zn充分反应,生成11.2 g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,16 g O3气体含有氧原子数为NA
B.标准况状下,44.8 L四氯化碳含有的分子数为2NA
C.0.1 mol·L-1氯化铝溶液中含有Al3+数为0.1NA
D.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
N0为阿伏加德罗常数的值。下列叙述正确的是( )
A.1.0 L pH=1的H2SO4溶液中所含H+数为0.2N0
B.26 g CH===CH(聚乙炔)所含碳碳单键数为2N0
C.1 mol Al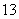 团簇离子的最外层电子总数为40N0
团簇离子的最外层电子总数为40N0
D.标准状况下,22.4 L CO、CO2混合气体中所含碳原子数为2N0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com