
分析 (1)Fe3+遇到KSCN溶液呈红色;
(2)Cu2O遇到酸生成Cu和硫酸铜,无Fe3+所以溶液也不变红;
(3)铜不溶于稀硫酸,所以铜只能被铁离子氧化;
(4)依据题意,能发生反应的物质为Cu2O,最后变成CuO,增加的质量就是反应的氧气的质量,根据质量差计算可以得出Cu2O的质量分数.
解答 解:(1)若假设1成立,Fe2O3与稀硫酸反应生成Fe3+,固体溶解遇到KSCN溶液呈红色,
故答案为:固体全溶,溶液变为血红色.
(2)由资料知Cu2O溶于稀硫酸生成Cu和CuSO4,铜为红色固体不溶水,铜离子的颜色为蓝色所以溶液变蓝,因溶液中无Fe3+所以滴加KSCN试剂也不变红,
故答案为:有红色固体生成,溶液变蓝,加入KSCN时,溶液不变红色;
(3)因为Cu2O溶于硫酸生成Cu和CuSO4,而H2SO4不能溶解Cu,所以混合物中必须有Fe2O3存在,使其生成的Fe3+溶解产生的Cu,若固体全部溶解,则一定存在Fe2O3和Cu2O,涉及的反应有Fe2O3+6H+═2Fe3++3H2O、Cu2O+2H+=Cu2++Cu+H2O、2Fe3++Cu═2Fe+Cu2+,
故答案为:3;Fe2O3+6H+═2Fe3++3H2O,Cu2O+2H+=Cu2++Cu+H2O,2Fe3++Cu═2Fe+Cu2+.
(4)依据题意,能发生反应的物质为Cu2O,最后变成CuO,增加的质量就是反应的氧气的质量,根据质量差计算可以得出Cu2O的质量分数.
设样品中氧化亚铜的质量为m,
2Cu2O+O2═4CuO△m
288g 32g
m (b-a)g
m=$\frac{288(b-a)g}{32g}$=9(b-a)g,
混合物中Cu2O的质量分数为 $\frac{9(b-a)}{a}$×100%,
故答案为:$\frac{9(b-a)}{a}$×100%.
点评 本题考查实验的设计及评价,以及物质的组成及含量的测定,本题难度中等,做题时要特别重视题干所给给信息的应用,掌握基础是关键.


科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 9种 | C. | 12种 | D. | 15种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6 g CH4中含有的C-H键数目为0.4 NA | |
| B. | 0.1 mol CaO2中含有的阴、阳离子总数为0.2 NA | |
| C. | 加热条件下足量的铜粉与含0.2 mol H2SO4的浓硫酸充分反应,转移电子数目为0.2 NA | |
| D. | 标准状况下,2.24 L H37Cl含有的中子数为2.0 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | X | Y | Z | M |
| A | H2SO4(浓) | Fe2(SO4)3 | FeSO4 | Fe |
| B | O2 | CO2 | CO | C |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
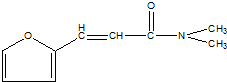 是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )
是一种高效麻醉剂,该有机物同分异构体中含有羧基(-COOH)和氨基(-NH2),且苯环上有2个取代基的有(不考虑立体异构)( )| A. | 12种 | B. | 15种 | C. | 18种 | D. | 21种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 次氯酸钙溶液中通入过量二氧化碳:ClO-+H2O+CO2═HCO3-+HClO | |
| B. | 过量的NaHSO4与Ba(OH)2溶液反应:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O | |
| C. | 硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+═Fe3++4H2O | |
| D. | 硝酸铁溶液中加过量氨水:Fe3++3NH3•H2O═Fe(OH)3↓+3NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
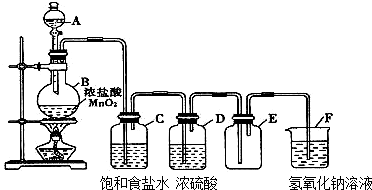
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CCl4、SiCl4、SiH4 | B. | H2S、NF3、CH4 | C. | BCl3、NH3、CO2 | D. | SO3、BF3、H3O+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com