
0.1mol/LNaOH溶液和0.1mol/LNH4Cl溶液等体积混合后,溶液中离子浓度大小顺序正确的是
A.c(Na+)>c(Cl-)>c(OH-)>c(H+) B.c(Na+)=c(Cl-)>c(H+)>c(OH-)
C.c(Cl-)>c(Na+)>c(OH-)>c(H+) D.c(Na+)=c(Cl-)>c(OH-)>c(H+)
科目:高中化学 来源: 题型:
已知
NaCl(s)+H2SO4(浓)===NaHSO4+HCl↑
现在117 g NaCl晶体和足量的浓硫酸完全反应。求:
(1)产生的HCl在标准状况时的体积为多少?
(2)将所得HCl气体溶于100 g水中,若所得盐酸的密度为1.1 g·cm-3,则盐酸的物质的量浓度为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4·H2C2O4·2H2O(已知:KHC2O4·H2C2O4·2H2O的氧化产物为CO2,H2C2O4为二元弱酸)。若用0.100 0 mol·L-1的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L-1)为
A.0.008889 B.0.0800 C.0.1200 D.0.2400
查看答案和解析>>
科目:高中化学 来源: 题型:
用0.1 mol/LNaOH溶液滴定0.1 mol/L盐酸溶液,如达到滴定终点时不慎多加了1滴NaOH溶液 (1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH是( )
A.10 B.9 C.11.5 D.12.5
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在一个容积为2 L的密闭容器中加入0.8 mol A2气体和0.6 mol B2气体反应达平衡生成1mol AB气体并释放出热量,反应中各物质的浓度随时间的变化情况如图所示。下列说法不正确的是
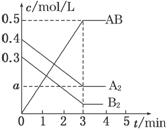
A.图中a点的值为0.15 B.该反应的平衡常数K=0.03
C.温度升高,平衡常数K值减小 D.平衡时A2的转化率为62.5%
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化合物:①HCl、 ②NaOH 、③CH3COOH 、④NH3·H2O、 ⑤CH3COONa 、⑥NH4Cl
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号)。
(2)常温下0.01mol/L HCl溶液的PH= ;PH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(3)将等PH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的PH仍相等,则m n (填“大于、等于、小于”)。
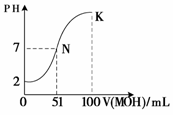 (4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
(4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:
①N点对应的溶液中,c(M+) c(A-)(填“大于、等于、小于”)。
②K点对应的溶液中,c(M+)+c(MOH)= mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
理论上不能设计原电池的化学反应是( )
A.CH4+2O2―→CO2+2H2O
B.HNO3+NaOH===NaNO3+H2O
C.2H2+O2===2H2O
D.2FeCl3+Fe===3FeCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
你认为减少酸雨产生的途径可采用的措施是( )
①少用煤作燃料 ②把工厂烟卤造高 ③燃料脱硫 ④在已酸化的土壤中加石灰 ⑤开发新能源
A.①②③ B.②③④⑤
C.①③⑤ D.①③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com