
下列说法不正确的是( )
A.元素周期表是元素周期律的具体表现形式
B.元素周期表中行和列一样多
C.元素周期表中,某一列内所含元素的种数可能跟某一行中所含元素的种数相等
D.元素周期表中周期数等于该周期内原子的电子层数
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
苏丹红一号(sudan Ⅰ)是一种偶氮染料,不能作为食品添加剂使用。它是由苯胺和2萘酚为主要原料制备的,它们的结构简式如图所示:
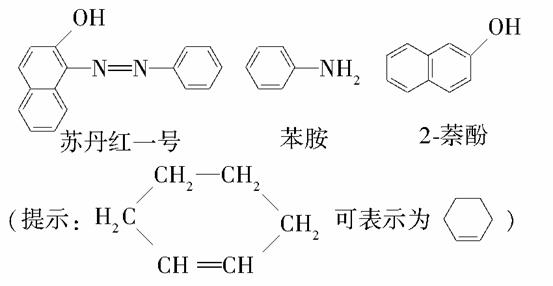 (1)苏丹红一号的分子式为_______________________________。
(1)苏丹红一号的分子式为_______________________________。
(2)在下面化合物A~D中,与2萘酚互为同分异构体的有(填字母代号)________。

(3)上述化合物C含有的官能团的名称是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电子云的叙述中,正确的是( )
A.电子云形象地表示了电子在核外某处单位体积内出现的概率
B.电子云直观地表示了核外电子的数目
C. 1s电子云界面图是一个球面,表示在这个球面以外,电子出现的概率为零
D.电子云图中的小黑点表示了电子运动的轨迹
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 | 元素性质或原子结构 |
| T | M层上有2对成对电子 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(1)元素T的原子最外层共有________种不同运动状态的电子。元素X的一种同位素可测定文物年代,这种同位素的符号是_______。
(2)元素Y与氢元素形成一种离子YH ,写出该微粒的电子式 ________(用元素符号表示)。
,写出该微粒的电子式 ________(用元素符号表示)。
(3)元素Z与元素T相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)探寻物质的性质差异性是学习的重要方法之一。T、X、Y、Z四种元素的最高价氧化物对应的水化物中化学性质明显不同于其他三种酸的是________,理由是:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.元素的种类由原子的质量数决定
B.原子的种类由原子核内质子数与中子数共同决定
C.核外电子排布相同的两个原子一定是同种原子
D.某元素的原子核内有m个质子,n个中子,则该元素的相对原子质量为m+n
查看答案和解析>>
科目:高中化学 来源: 题型:
下列给出14种元素的电负性:
| 元素 | Al | B | Be | C | Cl | F | Li | Mg | N | Na | O | P | S | Si |
| 电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 | 1.2 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
请运用元素周期律知识完成下列各题。
(1)同一周期中,从左到右,元素的电负性逐渐________;同一主族中,从上到下,元素的电负性逐渐________。所以,元素的电负性随原子序数的递增呈________变化。
(2)短周期元素中,由电负性最大的元素与电负性最小的元素形成的化合物的化学式为________,用电子式表示该化合物的形成过程:____________________________________。
(3)表中符合“对角线规则”的元素有Li和________、Be和________、B和________,它们的性质分别有一定的相似性,其原因是____________________,写出Be(OH)2与强酸及强碱反应的离子方程式:____________________________________。
(4)一般认为,两成键元素间电负性差值大于1.7时形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。判断Mg3N2、SO2、AlCl3、CS2、MgO是离子化合物还是共价化合物。
离子化合物___________________________________________
共价化合物___________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
CO2气体在一定条件下可与金属镁反应,干冰在一定条件下也可以形成CO2气体,这两个变化过程中需要克服的作用力分别是( )
A.化学键,化学键
B.化学键,分子间作用力
C.分子间作用力,化学键
D.分子间作用力,分子间作用力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com