
| A�� | ��ȡ8gNaOH���壬����100mL��Ͳ�У��߽����������������ˮ����������ȫ�ܽ��������ˮϡ����100mL | |
| B�� | ��ȡ8gNaOH���壬����100mL����ƿ�У�������������ˮ��������ƿʹ�����ܽ⣬�ټ���ˮ���̶ȣ��Ǻ�ƿ��������ҡ�� | |
| C�� | ��ȡ8gNaOH���壬����100mL�ձ��У����ձ��м�������ˮ��ͬʱ���Ͻ����������ܽ� | |
| D�� | ��100mL��Ͳ��ȡ40ml 5mol/L NaOH��Һ��ϡ�ͺ�ת����100ml����ƿ�У�ϴ�Ӳ����� |
���� A����ͲΪ������������������������Һ��
B������ƿΪ�������������������ܽ���壻
C�����ܽ��ձ��м�������ˮ���������Ƶ���Һ�������100mL��Ũ�Ȳ���2mol/L��
D.40mL5mol/L NaOH��Һϡ�ͳ�100mL��Һ��ϡ�ͺ����ҺŨ��ԼΪ2mol/L��
��� �⣺A����ͲΪ������������������������Һ��Ӧ������ƿ�н��У���A����
B������ƿΪ�������������������ܽ���壬Ӧ���ձ����ܽ⣬Ȼ��ת�Ƶ�����ƿ�����ƣ���B����
C�����ձ��м�������ˮ��������100mL�̶��ߣ����Ƶ���Һ���������100mL��Ũ��Ҳ����2mol/L����C����
D.100mL2mol•L-1 ��NaOH��Һ�����������Ƶ����ʵ�����0.2mol��40mL5mol•L-1��NaOH��Һ�����������Ƶ����ʵ�����0.2mol��������Һ���ʵ����ʵ�����ȣ��������������ʵ���Ũ��ԼΪ2mol•L-1 NaOH��Һ100mL����D��ȷ��
��ѡ��D��
���� ���⿼��������һ�����ʵ���Ũ�ȵ���Һ��������Ŀ�ѶȲ������ص㿼����Ͳ������ƿ���ձ���ʹ�ã�ע���ܽ��ϡ����Һ��Ӧ�����ձ��н��У���������Ͳ������ƿ�н��У�ע����������һ�����ʵ���Ũ�ȵķ�����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������ڵ�IA�� | B�� | �������ڵ�IA�� | C�� | �������ڵ�IA�� | D�� | �ڶ����ڵ�IIA�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼����þ��Һ�м�������Ca��OH��2��Һ��Mg2++HCO3-+Ca2++2OH-=MgCO3��+CaCO3��+2H2O | |
| B�� | SO2����ͨ��Fe2��SO4��3��Һ�У�SO2+2H2O+2Fe3+=2Fe2++4H++SO42- | |
| C�� | �ð״׳����⣺Fe2O3•xH2O+6H+=��3+x��H2O+2Fe3+ | |
| D�� | ���������Һ�еμ�����NaOH��Һ��H++NH4++2OH-=NH3•H2O+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
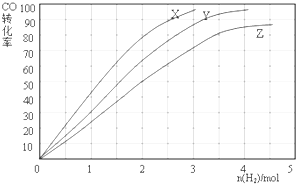
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ܹ����������˶� | B�� | �������Ӵ���� | ||
| C�� | ��������ֱ����1-100nm֮�� | D�� | �������Ӳ��ܴ�����Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2 | B�� | Na2O | C�� | NaClO | D�� | FeSO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
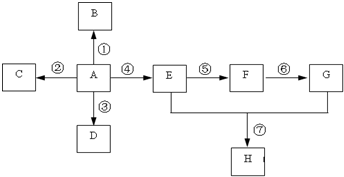 ��֪A��һ����Ҫ�Ļ�������ԭ�ϣ��������̼Ԫ�صİٷֺ���Ϊ85.7%������Է�����С��30��A��B��C��D��E��F��G��H����ͼ��ʾ��ת����ϵ�����ֲ�������ȥ��������BΪ�߷��ӻ����CΪ��ɫ��ζ���壬ʵ�����п���ͨ��G�����ʯ��ȡ��DΪ��������ʹ���Ը��������Һ��ɫ��E��GΪ�����г������л����E��������ζ��H����ζ��
��֪A��һ����Ҫ�Ļ�������ԭ�ϣ��������̼Ԫ�صİٷֺ���Ϊ85.7%������Է�����С��30��A��B��C��D��E��F��G��H����ͼ��ʾ��ת����ϵ�����ֲ�������ȥ��������BΪ�߷��ӻ����CΪ��ɫ��ζ���壬ʵ�����п���ͨ��G�����ʯ��ȡ��DΪ��������ʹ���Ը��������Һ��ɫ��E��GΪ�����г������л����E��������ζ��H����ζ��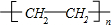 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
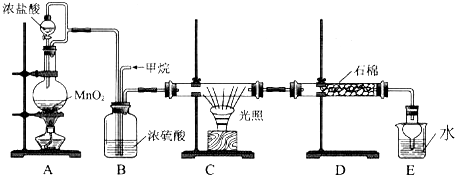
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
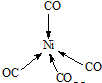 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com