
| A. | 稀释前,c (A)>10 c (B) | |
| B. | 稀释前,A溶液中水电离出的OH- 浓度是B溶液中由水电离出的OH- 浓度的10倍 | |
| C. | 在M点,A、B两种碱溶液中阳离子的物质的量浓度相等 | |
| D. | M点时A和B的浓度相等 |
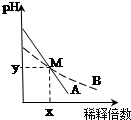
分析 室温下pH相差1的两种一元碱溶液A和B,根据图象可知:稀释相同倍数x时两溶液的pH相等,说明AOH的碱性大于BOH,
A.依据图象分析判断AB稀释相同倍数,A的pH变化大,
B.稀释前A溶液中氢氧根离子浓度大于B溶液中;碱是抑制水的电离;
C.M点AB溶液pH相同;
D.醋酸是弱酸和一元碱反应生成的盐溶液酸碱性由离子的水解程度决定,恰好反应溶液pH不为7.
解答 解:根据图象可知,室温下pH相差1的两种一元碱溶液A和B,稀释相同倍数(x倍)时两溶液的pH相等,说明AOH的碱性大于BOH,
A.稀释前,设c(AOH)=0.1mol/L,c(BOH)>0.01mol/L,则c(AOH)<10c(BOH),故A错误;
B.稀释前A溶液和B溶液中的pH分别是a+1,a则氢稀释前,A溶液离子浓度分别是10-(a+1)mol/L和10-amol/L,而碱溶液中氢离子都是由水电离出来,与水电离出的OH-的浓度相等,A溶液中由水电离出的OH-的浓度是B溶液中由水电离出的OH-的0.1倍,故B错误;
C.M点AB溶液pH相同,氢氧根离子浓度相同,所以M点A、B两种碱溶液中阳离子的物质的量浓度相等,故C正确;
D.M点AB溶液pH相同,而A的电离度远大于B,所以浓度B大于A的浓度,故D错误;
故选C.
点评 本题考查电解质在水中的电离及图象,题目难度中等,明确图象中pH的变化及交点的意义是解答本题的关键,注意掌握弱电解质的电离平衡及其影响.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 整个过程中,H20的电离度逐渐增大 | B. | c(Na+)>c(HS-)>c(H+)>c(S2-)>c(0H-) | ||
| C. | c(Na+)+c(H+)═c(0H-)+c(HS-)+2c(S2-) | D. | c(Na+)═c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LCO中一定含有6.02×1023个分子 | |
| B. | 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10NA | |
| C. | 常温常压下,16gO2与16gO3含有的分了数相同 | |
| D. | 0.1mol/LK2SO4溶液中含有K+为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 为探究碳酸钠和碳酸氢钠固体的热稳定性,某同学设计了“套管实验”,装置如图,大试管A与小试管a相连通,大试管B小试管b相连通.
为探究碳酸钠和碳酸氢钠固体的热稳定性,某同学设计了“套管实验”,装置如图,大试管A与小试管a相连通,大试管B小试管b相连通.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com