
【题目】锂—铜空气燃料电池(如图)容量高、成本低,该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为:2Li+Cu2O+H2O=2Cu+2Li++2OH-,下列说法错误的是

A. 整个反应过程中,氧化剂为O2
B. 放电时,正极的电极反应式为:Cu2O+H2O+2e-=2Cu+2OH-
C. 放电时,当电路中通过0.1 mol电子的电量时,有0.1 mol Li+透过固体电解质向Cu极移动,有标准状况下1.12 L氧气参与反应
D. 通空气时,铜被腐蚀,表面产生Cu2O
【答案】C
【解析】A,根据题意,该电池通过一种复杂的铜腐蚀“现象”产生电力,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,由放电反应推知Cu极电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,Cu2O又被还原成Cu,整个过程中Cu相当于催化剂,氧化剂为O2,A项正确;B,放电时正极的电极反应式为Cu2O+2e-+H2O=2Cu+2OH-,B项正确;C,放电时负极电极反应式为Li-e-=Li+,电路中通过0.1mol电子生成0.1molLi+,Li+透过固体电解质向Cu极移动,反应中消耗O2物质的量为![]() =0.025mol,在标准状况下O2的体积为0.025mol
=0.025mol,在标准状况下O2的体积为0.025mol![]() 22.4L/mol=0.56L,C项错误;D,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,D项正确;答案选C。
22.4L/mol=0.56L,C项错误;D,放电过程中消耗Cu2O,由此可见通入空气Cu腐蚀生成Cu2O,D项正确;答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】金属氢氧化物在酸中溶解度不同,因此可以利用这一性质,控制溶液的pH,达到分离金属离子的目的。难溶金属的氢氧化物在不同pH下的溶解度(S/mol/L)如图所示。

(1)当pH=3时,溶液中铜元素的主要存在形式是__________。
(2)若要除去CuCl2溶液中的少量Fe3+,应该控制溶液的pH值为______ (填序号)。
A.<1 B.4左右 C.8>PH>6 D.>9
(3)在Ni(NO3)2溶液中含有少量的Co2+杂质,________(填“能”或“不能”)通过调节溶液pH的方法来除去,理由是_____________________________________________。
(4)已知一些难溶电解质的溶度积常数如右下表:
物质 | FeS | MnS | PbS | HgS | ZnS | CuS |
Ksp | 6.3×10-18 | 2.5×10-13 | 3.4×10-28 | 6.4×10-33 | 1.6×10-24 | 1.3×10-35 |
为除去某工业废水中含有的Cu2+、Pb2+、Hg2+杂质,最适宜向此工业废水中加入过量的___________(填序号)。
A.NaOH B.FeS C.Na2S D.NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.1 mol氦气所含原子的数目为2NA
B.12 g 12C中所含的碳原子数为NA
C.标况下22.4 L的任何气体所含原子数均为NA
D.相同体积的O2(g)和NO2(g)分子数均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下图所示装置:
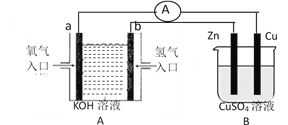
(1)装置A中b的电极名称为________极,a电极反应式为___________________________________;
(2)B装置中Cu为________极,电极反应式为___________________________________;
(3)当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为______________ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下有浓度均为0.1 mol![]() 的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
的四种溶液:①Na2CO3 ②NaHCO3 ③HCl ④NH3·H2O
(1)有人称溶液①是油污的“清道夫”,原因是_____________________(用离子方程式解释)
(2)这四种溶液中水的电离程度由大到小的顺序是(用序号填写)______________________
(3)向④中加入少量氯化铵固体,此时![]() 的值___________(填“增大”“减小”或“不变”)。
的值___________(填“增大”“减小”或“不变”)。
(4)等体积混合③和④的溶液,此时溶液中[NH4+]+[NH3·H2O]=_____________mol·L-1(填数值);此时溶液中离子浓度的大小顺序是:__________________________;若将③和④的溶液混合后溶液恰好呈中性,则混合前③的体积_________④的体积(填“大于”小于”或“等于”)
(5)将10 mL溶液③加水稀释至100 mL,则此时溶液中由水电离出的c( H+)=___________ mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列混合溶液中,各离子浓度的大小顺序正确的是
A. 10L0.1mol·L-1氨水与10L0.1mol·L-1盐酸混合:[Cl-]>[NH4+]>[OH-]>[H+]
B. 10mL0.1mol·L-1NH4Cl溶液与5mL0.2mol·L-1NaOH溶液混合:[Na+]=[Cl-]>[OH-]>[H+]
C. 10mL0.1mol·L-1CH3COOH溶液与5mL0.2mol·L-1NaOH溶液混合:[Na+]=[CH3COO-]>[OH-]>[H+]
D. 10mL0.5mol·L-1CH3COONa溶液与6mL1mol·L-1盐酸混合:[Cl-]>[Na+]>[OH-]>[H+]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为元素周期表的一部分,请根据元素①~⑧在表中的位置,用化学用语回答下列问题:
族 周期 | IA | 0 | ||||||
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)在上述元素的最高价氧化物对应的水化物中:属于强酸的是________(用化学式表示,下同);碱性最强的是________。
(2)④、⑤、⑥的简单离子半径由大到小的顺序是________(用离子符号)。
(3)由①、④、⑤、三种元素组成的化合物中化学键的类型有:________。
(4)请写出涉及上述有关元素的两个置换反应(要求:同一反应中两种单质对应元素既不同周期也不同主族)________;__________。
(5)由表中元素形成的常见无机化合物A、B、C、X有以下转化关系:
A![]() B
B![]() C
C
若A、B、C含同一金属元素,X为强电解质,且反应都在溶液中进行.B的化学式为______。对应的反应①的离子方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子晶体:
①HCl ②HBr ③HI ④CO ⑤N2 ⑥H2
熔沸点由高到低的顺序是
A.①②③④⑤⑥ B.③②①⑤④⑥ C.③②①④⑤⑥ D.⑥⑤④③②①
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com