
下图是元素周期表的一部分,下列说法正确的是( )

A.可在灰色区域“甲”中寻找催化剂
B.离子半径:W-﹥Y3-﹥X+
C.气态氢化物的稳定性:Z﹥W
D.工业上电解X和W化合物的水溶液制备X
科目:高中化学 来源:2013-2014学年江苏省高三年级模拟考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述正确的是
A.标准状况下,2.24 L 水中所含电子总数为NA
B.1 L 0.2 mol·L-1硫酸铁溶液中含有的SO42-数为0.2NA
C.苯和苯甲酸混合物1 mol,完全燃烧消耗O2的分子数为7.5NA
D.标准状况下,7.1 g氯气与足量石灰乳充分反应转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省茂名市高三第二次高考模拟理综化学试卷(解析版) 题型:实验题
氨水是一种的常用的化学试剂。
(1)以浓氨水和生石灰为原料,用如下装置为发生装置,可制取少 量氨气。已知:NH3·H2O+CaO=Ca(OH)2+NH3↑。

①生石灰应该装在 (填A或B)。
②试从电离平衡角度分析该实验中氨气逸出的原因: 。
③现要用试管和必要实验用品收集一试管氨气,请在C处补充相应收集装置。
(2)化学兴趣小组用氨水与硝酸银溶液配制好银氨溶液后,进行乙醛的银镜反应实验,但部分同学实验时间长,且效果不明显。影响乙醛银镜反应速率的因素有哪些呢?请你完成如下猜想:
①猜想:因素一:银氨溶液的pH大小;
因素二: 。
②你设计实验验证上述影响因素一,完成下表中内容。
提供试剂:乙醛、2%稀氨水、 0.25mol/L NaOH溶液、盐酸 、 2% AgNO3溶液
实验用品:烧杯(装有热水)、试管
实验步骤 | 实验操作 | 预期现象及结论(步骤1只填现象) |
1 | 在A、B两支洁净的试管中各入1mL 2%的AgNO3溶液,然后边振荡试管边逐滴滴入2%稀氨水,至最初产生的沉淀恰好完全溶解,此时制得pH均约为8的银氨溶液。 |
|
2 |
|
|
(3)吸取20.00ml 上述氨水于锥形瓶,滴加3滴甲基橙指示剂,用0.0050mol/L标准硫酸滴定,滴定至出现红色为终点,重复3次实验,平均消耗标准硫酸20.04 ml,计算上述氨水的物质的量浓度
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省肇庆市高三级第一次模拟考试理综化学试卷(解析版) 题型:选择题
在0.1mol/L的Na2CO3的溶液中,下列关系式正确的是
A.c(Na+)>c(CO32-)> c(OH-)> c(H+)
B.c(OH-)= c(HCO3-)+ c(H2CO3)
C.2c(Na+)=c(CO32-)+ c(HCO3-)> c(H2CO3)
D.c(Na+)+ c(H+)= c(OH-) + c(HCO3-) +2c(CO32-)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省潮州市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ. AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用试剂:KSCN溶液、NaOH溶液、氯水、KMnO4溶液。
⑴请完成下表:
操作 | 现象 | 结论 |
取少量除尽Ag+后的溶液于试管中,加入 ,振荡 |
| 存在Fe3+ |
取少量除尽Ag+后的溶液于试管中,加入1~2滴KMnO4溶液,振荡 |
| 存在Fe2+ |
【实验结论】Fe的氧化产物为存在Fe2+和Fe3+
Ⅱ. AgNO3的热稳定性
用下图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。
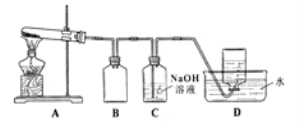
Ⅱ.⑵装置B的作用是 。
⑶经小组讨论并验证该无色气体为O2,其验证方法是 。
⑷【查阅资料】Ag2O和粉末的Ag均为黑色;Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:① Ag;② Ag2O;③ Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验。
实验编号 | 操作 | 现象 |
a | 加入足量氨水,振荡 | 黑色固体不溶解 |
b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验评价】根据上述实验,不能确定固体产物成分的实验是 (填实验编号)。
【实验结论】根据上述实验结果,得出AgNO3固体受热分解的方程式为 。
【实验拓展】取2.0g AgNO3样品充分受热分解,共收集到标况下气体的体积为336mL,则样品中AgNO3的百分含量为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省潮州市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列条件下,离子能大量共存或者离子方程式正确的是
A.pH=1的溶液中:Fe2+、ClO-、Na+、SO42-
B.在含较多Al3+的溶液中:K+、Cl-、HCO3-
C.一小块钠投入到CuSO4溶液中:2Na+Cu2+= Cu+2Na+
D.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省清远市高三4月模拟理综化学试卷(解析版) 题型:选择题
25℃时,某浓度的NH4Cl溶液pH = 4,下列叙述正确的是
A.溶液中的 c(OH-) = 1×10-10 mol·L-1
B.溶液中的c(NH4+)>c(Cl-)>c(H+)>c(OH-)
C.溶液中的c(H+) + c(NH4+) = c(Cl-) + c(OH-)
D.溶液中的c(NH3·H2O) = c(NH4+)
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省深圳市高三第二次调研考试理综化学试卷(解析版) 题型:选择题
下列各组离子在水溶液中能大量共存的是( )
A.Na+、HCO3-、SO32-、OH- B.Al3+、H+、SiO32-、I-
C.Fe2+、K+、NO3-、SO42- D.Fe3+、NH4+、ClO-、CO32-
查看答案和解析>>
科目:高中化学 来源:2013-2014学年广东省十校联考高三下学期理综化学试卷(解析版) 题型:选择题
下列实验“操作和现象”与“结论”对应关系正确的是
| 操作和现象 | 结论 |
A | 常温下将Al片放入浓硝酸中,无明显变化 | Al与浓硝酸不反应 |
B | 向0.1mol·L-1 Na2CO3溶液中,滴加2滴酚酞显浅红色,微热, 红色加深。 | 说明盐类水解是吸热反应 |
C | 向FeCl3溶液加入足量的铜粉,充分反应,静置,取上层清液 滴加几滴KSCN溶液,溶液不变血红色。 | 说明氧化性:Fe3+>Cu2+ |
D | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液,有白色沉淀生成 | 该溶液中一定含有SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com