
| A、有白色絮状沉淀产生,且不溶解 |
| B、先有白色絮状沉淀,后又溶解 |
| C、一直无明显现象 |
| D、先无现象,后有白色絮状沉淀 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、1mol CO2的体积约是22.4L |
| B、1mol氦气中含有2NA个原子 |
| C、0.3molN2、0.7molO2的混合气体在标准状况下的体积约为22.4L |
| D、1mol H2SO4所含粒子数为NA个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
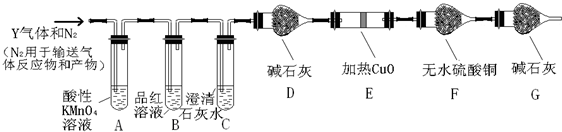
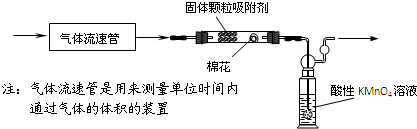
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 待提纯物质 | 杂质 | 除杂试剂及主要操作方法 |
| A | 苯 | 溴单质 | 加亚硫酸钠溶液洗涤,分液 |
| B | 淀粉 | 葡萄糖 | 水,过滤 |
| C | 甲烷 | 乙烯 | 通入酸性高锰酸钾溶液,洗气 |
| D | 乙酸乙酯 | 乙酸 | 加入氢氧化钠溶液,分液 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
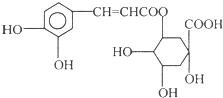 下列关于该化合物的说法不正确的是( )
下列关于该化合物的说法不正确的是( )| A、1mol绿原酸最多可与4mol NaOH发生反应 |
| B、与乙醇发生酯化反应后的有机物分子式为C18H24O9 |
| C、1mol绿原酸最多可与4 mol Br2发生反应 |
| D、能发生加成、取代、氧化、消去反应,也能发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
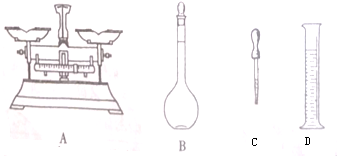
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①②④⑤ |
| C、②④⑤⑥ | D、②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2溶于水生成碳酸,SiO2不溶于水也不能跟水直接反应生成硅酸 | ||||
B、在高温条件下,SiO2和Na2CO3能发生反应:SiO2+Na2CO3
| ||||
| C、SiO2熔点比CO2高 | ||||
| D、CO2通入Na2SiO3稀溶液中,生成的H2SiO3逐渐聚合而形成硅酸溶胶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com