
分析 (1)Fe和稀盐酸反应生成氯化亚铁和氢气,Cu不反应,然后过滤洗涤得到Cu;
(2)Fe、Cu混合物中加入少量硫酸铜溶液并搅拌,Fe和硫酸铜反应生成硫酸亚铁和Cu,然后过滤洗涤得到Cu;
最好的方法是采用物理方法将这两种物质分开且操作方便.
解答 解:(1)Fe和稀盐酸反应生成氯化亚铁和氢气,Cu不反应,然后过滤洗涤得到Cu,该方法过程中生成氢气逸出,导致浪费资源;
(2)Fe、Cu混合物中加入少量硫酸铜溶液并搅拌,Fe和硫酸铜反应生成硫酸亚铁和Cu,然后过滤洗涤得到Cu,该方法去除了Fe而增加了Cu,比(1)好;
最好的方法是采用物理方法将这两种物质分开且操作方便,因为Fe能被磁铁吸引,所以可以用磁铁将Fe、Cu分开即可,且操作方便,
故答案为:(2);去除铁而增加了铜;用磁铁吸取铁屑.
点评 本题考查化学实验方案评价,为高频考点,侧重考查学生实验操作、实验分析评价能力,明确实验原理及物质性质差异性是解本题关键,注意:实验要遵循绿色化学、操作简便易行、实验药品经济的特点,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | F | Ne | |||
| 3 | Na | Al | P | S | Cl |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和乙炔属于不饱和烃,乙烷属于饱和烃 | |
| B. | 乙烯和乙炔分子中所有原子都在同一平面上,乙烷分子中所有原子不都在同一平面上 | |
| C. | 乙烯和乙炔都能发生加成反应,乙烷不能发生加成反应 | |
| D. | 在发生加成反应时,乙烯和乙炔分子中的碳碳键全部断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤ | B. | ②③④ | C. | ①②④⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
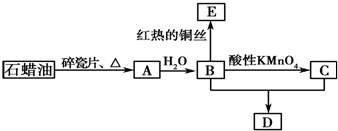
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀HNO3溶解FeS固体:FeS+2H+═Fe2++H2S↑ | |
| B. | 将Na2O2固体投入H218O中:2Na2O2+H218O═Na++4OH-+8O2↑ | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液,恰好使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+NH3•H2O+BaSO4↓ | |
| D. | 用石墨作两电极电解MgCl2溶液:2C1-+2H2O$\frac{\underline{\;电解\;}}{\;}$C12↑+2OH-+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com