
”¾ĢāÄæ”æŌŚĶØ·ē³÷ÖŠ½ųŠŠĻĀĮŠŹµŃé£ŗ
ŹµŃé ²½Öč |
|
|
|
|
ĻÖĻó | Fe±ķĆę²śÉś“óĮæ ĪŽÉ«ĘųĢ壬ŌŚŅŗĆę ÉĻ·½±äŗģ×ŲÉ« | Fe±ķĆęĪŽĆ÷ ĻŌ±ä»Æ | ³£ĪĀĻĀÓŠĪŽÉ«ĘųÅŻ£¬¼ÓČČŗó£¬Cu±ķĆę²śÉśĪŽÉ«ĘųĢ壬ŌŚŅŗĆęÉĻ·½±äŗģ×ŲÉ« | Cu±ķĆę²śÉśŗģ ×ŲÉ«ĘųĢå |
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©¢ŁÖŠĘųĢåÓÉĪŽÉ«±äĪŖŗģ×ŲÉ«£¬ŗģ×ŲÉ«ĘųĢåŹĒ__________________£ØĢī·Ö×ÓŹ½£©”£
£Ø2£©¢ŚÖŠµÄĻÖĻóĖµĆ÷Fe·¢ÉśĮĖ______ĻÖĻ󣬲śÉśµÄŌŅņŹĒ________________________”£
£Ø3£©¶Ō±Č¢Ł¢ŚÖŠµÄĻÖĻó£¬______£ØĢī”°ÄÜ”±»ņ”°²»ÄÜ”±£©ĖµĆ÷Ļ”ĻõĖįµÄŃõ»ÆŠŌĒæÓŚÅØĻõĖį”£
£Ø4£©¶Ō±Č¢Ū¢ÜÖŠµÄĻÖĻó£¬ĖµĆ÷Ńõ»ÆŠŌ£ŗĻ”ĻõĖį______£ØĢī”°>”±»ņ”°<”±£©ÅØĻõĖį”£
£Ø5£©¢ŪÖŠŌŚ¼ÓČČŹ±µÄ»Æѧ·“Ó¦·½³ĢŹ½ĪŖ________________________£¬“Ė·“Ó¦ÖŠĻ”ĻõĖį³ż±ķĻÖ³öŃõ»ÆŠŌĶā£¬»¹±ķĻÖ³ö____________”£
”¾“š°ø”æNO2 ¶Ū»Æ Fe±ķĆęŠĪ³ÉÖĀĆܵÄŃõ»ÆĤ£¬×čÖ¹Fe½ųŅ»²½·“Ó¦ ²»ÄÜ < ![]() ĖįŠŌ
ĖįŠŌ
”¾½āĪö”æ
£Ø1£©¢ŁÖŠµÄFeÓėĻ”ĻõĖį·¢Éś·“Ó¦£ŗ4HNO3(Ļ”)+Fe=Fe(NO3)3+NO”ü+2H2O£¬Éś³ÉµÄNOŌŚæÕĘųÖŠ±»Ńõ»Æ2NO+O2=2NO2£¬Éś³Éŗģ×ŲÉ«µÄNO2£¬¹Źŗģ×ŲÉ«ĘųĢåĪŖNO2£»
£Ø2£©¢ŚÖŠFe±ķĆęĪŽĆ÷ĻŌ±ä»Æ£¬ĖµĆ÷FeÓöÅØHNO3·¢Éś¶Ū»Æ£¬ŅņĪŖFeÓöÅØHNO3ŗó±ķĆęŠĪ³ÉÖĀĆܵÄŃõ»ÆĤ£¬×čÖ¹FeÓėÅØHNO3½ųŅ»²½·“Ó¦£»
£Ø3£©ÓÉÓŚFeÓėÅØHNO3»į·¢Éś¶Ū»Æ£¬²»ÄܽųŅ»²½·“Ó¦£¬ĖłŅŌ²»ÄÜ±Č½ĻÅØHNO3ŗĶĻ”HNO3µÄŃõ»ÆŠŌ£»
£Ø4£©Ļ”HNO3³£ĪĀĻĀ²»ÄÜÓėCu·“Ó¦£¬¶ųÅØHNO3³£ĪĀĻĀæÉŅŌÓėCu·“Ó¦£¬ĖµĆ÷Ļ”HNO3µÄŃõ»ÆŠŌŠ”ÓŚÅØHNO3£»
£Ø5£©CuÓėĻ”HNO3µÄ·“Ó¦ĪŖ£ŗ![]() £¬Ļ”ĻõĖį³ż±ķĻÖ³öŃõ»ÆŠŌĶā»¹Ęšµ½ĖįŠŌµÄ×÷ÓĆ”£
£¬Ļ”ĻõĖį³ż±ķĻÖ³öŃõ»ÆŠŌĶā»¹Ęšµ½ĖįŠŌµÄ×÷ÓĆ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±źŗÅĪŖ¢Ł”«¢āµÄŌŖĖŲ£¬ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĻĀ£ŗ
Ö÷×å ÖÜĘŚ | ¢ńA | ¢ņA | ¢óA | ¢ōA | ¢õA | ¢öA | ¢÷A | 0×å |
1 | ¢Ł | ¢Ś | ||||||
2 | ¢Ū | ¢Ü | ¢Ż | ¢Ž | ||||
3 | ¢ß | ¢ą | ¢į | ¢ā |
ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©(ĢīŠ“ŌŖĖŲ·ūŗÅ)¢Ł _____¢Ū______¢Ż_____ ¢ß_____
£Ø2£©¢ŁŗĶ¢ÜŗÅŌŖĖŲŠĪ³ÉµÄ»ÆŗĻĪļµÄ»ÆѧŹ½________£¬ÓƵē×ÓŹ½±ķŹ¾ĘäŠĪ³É¹ż³ĢĪŖ__________”£
£Ø3£©¢ßŗĶ¢ąŗÅŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄ¼īŠŌŹĒ£ŗ ______©_________ £ØĢī»ÆѧŹ½£©”£¢įŗĶ¢āŗÅŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĖįŠŌŹĒ£ŗ ______ ©_________ £ØĢī»ÆѧŹ½£©”£
£Ø4£©¢Ł”¢¢Ż”¢¢ßŗÅŌŖĖŲŠĪ³ÉµÄŅ»ÖÖ»ÆŗĻĪļµÄµē×ÓŹ½ŹĒ________£¬ŌŚøĆ»ÆŗĻĪļÖŠ¼Čŗ¬ÓŠ________¼ü£¬ÓÖŗ¬ÓŠ________¼ü”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŹµŃ銔×éĶ¬Ń§ĄūÓĆŅŌĻĀ×°ÖĆÖʱø°±Ęų£¬²¢Ģ½¾æ°±ĘųµÄŠŌÖŹ(²æ·ÖŅĒĘ÷ŅŃĀŌČ„)”£Ēė»Ų“š£ŗ
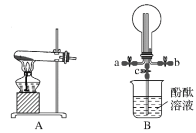
£Ø1£©ŹµŃéŹŅÖʱø°±ĘųµÄ»Æѧ·½³ĢŹ½ĪŖ__”£
£Ø2£©ŌŚÖĘČ”°±Ęųŗó£¬Čē¹ūŅŖøÉŌļ°±Ęų£¬æÉŃ”ÓƵÄøÉŌļ¼ĮŹĒ__”£
A.¹ĢĢåĒāŃõ»ÆÄĘ
B.ÅØĮņĖį
C.ĀČ»ÆøĘ
D.ĪåŃõ»Æ¶žĮ×
E.¼īŹÆ»Ņ
£Ø3£©ÓĆ×°ÖĆBŹÕ¼Æ°±ĘųŹ±£¬°±ĘųµÄ½ųĘųæŚŹĒ___(Ģī”°a”±»ņ”°b”±)”£
£Ø4£©“żŌ²µ×ÉÕĘæÖŠŹÕ¼ÆĀś°±Ęųŗ󣬹Ų±Õa”¢b£¬“ņæŖ×°ÖĆBÖŠµÄÖ¹Ė®¼Šc£¬Ņ»¶ĪŹ±¼äŗó£¬Čō¹Ū²ģµ½ÉÕĘæÄŚ²śÉśĮĖŗģÉ«ÅēČŖ£¬ŌņĖµĆ÷°±Ęų¾ßÓŠµÄŠŌÖŹŹĒ£ŗ___”¢___”£
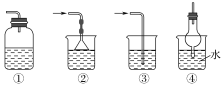
£Ø5£©ŅŌĻĀ×°ÖĆ(Ź¢·ÅµÄŅŗĢå¾łĪŖĖ®)æÉÓĆÓŚĪüŹÕ¶ąÓą°±ĘųµÄŹĒ__(ĢīŠņŗÅ)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æA”¢B”¢C”¢D”¢E”¢FĪŖ֊ѧ»Æѧ³£¼ūµÄµ„ÖŹ»ņ»ÆŗĻĪļ£¬ĘäÖŠA”¢FĪŖµ„ÖŹ£¬³£ĪĀĻĀ£¬EµÄÅØČÜŅŗÄÜŹ¹Ģś”¢ĀĮ¶Ū»Æ£¬Ļą»„×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£ØĢõ¼žŅŃĀŌČ„£©”£Ķź³ÉĻĀĮŠĪŹĢā£ŗ
£Ø1£©ČōAĪŖµ»ĘÉ«¹ĢĢ壬BĪŖĘųĢ壬FĪŖ·Ē½šŹōµ„ÖŹ”£
¢ŁŠ“³öE×Ŗ±äĪŖCµÄ»Æѧ·½³ĢŹ½_____”£
¢ŚBŌŚæÕĘųÖŠÄÜŹ¹ŅųĘ÷±ķĆꏧȄ½šŹō¹āŌó”¢Öš½„±äŗŚ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
£Ø2£©ČōBĪŖÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ唣
¢ŁAµÄµē×ÓŹ½ĪŖ_____”£
¢Ś×ö¹żŅų¾µ·“Ó¦ŗóµÄŹŌ¹ÜæÉÓĆEµÄĻ”ČÜŅŗĒåĻ“£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_____”£
¢ŪŌŚøÉŌļדĢ¬ĻĀ£¬Ļņ¢Ś·“Ó¦µĆµ½µÄČÜÖŹÖŠĶØČėøÉŌļµÄĀČĘų£¬µĆµ½N2O5ŗĶŅ»ÖÖĘųĢåµ„ÖŹ£¬Š“³ö·“Ó¦µÄ»Æѧ·½³ĢŹ½_____”£

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”ææĘѧ¼ŅŅ»Ö±ÖĀĮ¦ÓŚ”°ČĖ¹¤¹ĢµŖ”±µÄŃŠ¾æ£¬ĻÖŅŃÓŠ¶ąÖÖ·½·Ø”£
£Ø·½·ØŅ»£©1918Äź£¬µĀ¹ś»Æѧ¼Ņ¹ž²®Ņņ·¢Ć÷¹¤ŅµŗĻ³É°±£ØN2(g)+3H2(g)![]() 2NH3(g) H<0£©µÄ·½·Ø¶ųČŁ»ńŵ±“¶ū»Æѧ½±”£
2NH3(g) H<0£©µÄ·½·Ø¶ųČŁ»ńŵ±“¶ū»Æѧ½±”£
£Ø1£©Čō½«1molN2ŗĶ3molH2·ÅČė1LµÄĆܱÕČŻĘ÷ÖŠ£¬5minŗóN2µÄÅضČĪŖ0.8mol/L£¬Õā¶ĪŹ±¼äÄŚÓĆN2µÄÅØ¶Č±ä»Æ±ķŹ¾µÄ·“Ó¦ĖŁĀŹĪŖ_____mol/(L”¤min)”£
£Ø2£©ŌŚŅ»¶ØĪĀ¶ČĻĀµÄ¶ØČŻĆܱÕČŻĘ÷ÖŠ·¢ÉśÉĻŹö·“Ó¦£¬ĻĀĮŠŠšŹöÄÜĖµĆ÷·“Ó¦ŅŃ¾“ļµ½Ę½ŗāדĢ¬µÄŹĒ____”£
a. v(N2)Õż=3v(H2)Äę
b. ČŻĘ÷ÖŠĘųĢåµÄĆÜ¶Č²»Ėꏱ¼ä¶ų±ä»Æ
c. ČŻĘ÷ÖŠĘųĢåµÄ·Ö×Ó×ÜŹż²»Ėꏱ¼ä¶ų±ä»Æ
d. ČŻĘ÷ÖŠĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæ²»Ėꏱ¼ä¶ų±ä»Æ
£Ø3£©ŗĻ³É°±·“Ó¦µÄÉś²śĢõ¼žŃ”ŌńÖŠ£¬ÄÜÓĆĄÕĻÄĢŲĮŠŌĄķ½āŹĶµÄŹĒ________”£
¢ŁŹ¹ÓĆ“ß»Æ¼Į ¢ŚøßĪĀ ¢ŪøßŃ¹ ¢Ü¼°Ź±½«°±ĘųŅŗ»Æ“ÓĢåĻµÖŠ·ÖĄė³öĄ“
A. ¢Ł¢Ū B. ¢Ś¢Ū C. ¢Ū¢Ü D. ¢Ś¢Ü
£Ø·½·Ø¶ž£©1998Äź£¬Į½Ī»Ļ£Ą°»Æѧ¼ŅĢį³öĮĖµē½āŗĻ³É°±µÄŠĀĖ¼Ā·£ŗ
£Ø4£©²ÉÓĆøßÖŹ×Óµ¼µēŠŌµÄSCYĢÕ“É(ÄÜ“«µŻH+)ĪŖ½éÖŹ£¬ŹµĻÖĮĖøßĪĀ(570”ę)³£Ń¹ĻĀøß×Ŗ»ÆĀŹµÄµē½ā·ØŗĻ³É°±£¬×Ŗ»ÆĀŹæÉ“ļµ½78£„£¬×°ÖĆČēĻĀĶ¼£ŗ
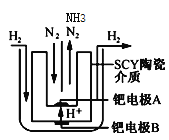
īŁµē¼«AŹĒµē½ā³ŲµÄ___¼«(Ģī”°Ńō”±»ņ”°Ņõ”±)£¬Ńō¼«·“Ó¦Ź½ĪŖ________”£
£Ø·½·ØČż£©×īŠĀµÄ”°ČĖ¹¤¹ĢµŖ”±ŃŠ¾æ±ØµĄ£ŗŌŚ³£ĪĀ”¢³£Ń¹”¢¹āÕÕĢõ¼žĻĀ£¬N2ŌŚ“߻ƼĮ±ķĆęÓėĖ®·¢Éś·“Ó¦£¬Ö±½ÓÉś³É°±ĘųŗĶŃõĘų£ŗ
ŅŃÖŖ£ŗN2(g)+3H2(g) ![]() 2NH3(g) ”÷H=£92 kJ£Æmol
2NH3(g) ”÷H=£92 kJ£Æmol
2H2(g)+O2(g)=2H2O(1) ”÷H=£571.6 kJ£Æmol
£Ø5£©Š“³öÉĻŹö¹ĢµŖ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½___________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚÖ÷×åŌŖĖŲX”¢Y”¢Z”¢MµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬XŌ×ÓŗĖĶā×īĶā²ćµē×ÓŹżŹĒĘäµē×Ó²ćŹżµÄ2±¶£¬X”¢YµÄŗĖĶā×īĶā²ćµē×ÓŹżÖ®±ČĪŖ2£ŗ3”£½šŹōµ„ÖŹZŌŚY2ÖŠČ¼ÉÕÉś³ÉµÄ»ÆŗĻĪļæÉÓėĖ®·¢ÉśŃõ»Æ»¹Ō·“Ó¦”£![]() µÄ×īĶā²ćĪŖ8µē×Ó½į¹¹”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ.
µÄ×īĶā²ćĪŖ8µē×Ó½į¹¹”£Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ.
£Ø1£©XµÄ×ī¼ņµ„Ēā»ÆĪļµÄ·Ö×ÓŹ½ĪŖ__________”£
£Ø2£©ZµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļŹōÓŚ_________£ØĢī”°Ėį”±»ņ”°¼ī”±£©”£
£Ø3£©ČČĪČ¶ØŠŌ£ŗXµÄ×ī¼ņµ„Ēā»ÆĪļ±ČYµÄ×ī¼ņµ„Ēā»ÆĪļ_______£ØĢī”°Ēæ”±»ņ”°Čõ”±£©”£
£Ø4£©½šŹōµ„ÖŹZŌŚY2ÖŠČ¼ÉÕÉś³É»ÆŗĻĪļ£¬1moløĆ»ÆŗĻĪļÓėĖ®·“Ó¦Ź±×ŖŅʵē×ÓŹżĪŖ_______mol”£
£Ø5£©Y”¢MĮ½ŌŖĖŲÖ®¼äŠĪ³ÉµÄ»ÆŗĻĪļ£¬³£ÓĆ×÷Ė®µÄĻū¶¾¼ĮµÄŹĒ_______£ØĢī·Ö×ÓŹ½£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ“×ĖįÄų[(CH3COO)2Ni]ŹĒŅ»ÖÖÖŲŅŖµÄ»Æ¹¤ŌĮĻ”£Ņ»ÖÖŅŌŗ¬Äų·ĻĮĻ£Øŗ¬NiS”¢Al2O3”¢FeO”¢CaO”¢SiO2£©ĪŖŌĮĻ£¬ÖĘČ”“×ĖįÄųµÄ¹¤ŅÕĮ÷³ĢĶ¼ČēĶ¼£ŗ
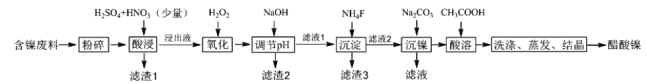
Ļą¹ŲĄė×ÓÉś³ÉĒāŃõ»ÆĪļµÄpHŗĶĻą¹ŲĪļÖŹµÄČܽāŠŌČē±ķ£ŗ
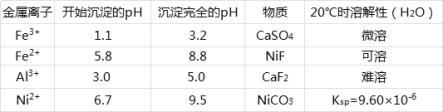
£Ø1£©Ėį½ž¹ż³ĢÖŠ£¬1mol NiSŹ§Č„6NAøöµē×Ó£¬Ķ¬Ź±Éś³ÉĮ½ÖÖĪŽÉ«ÓŠ¶¾ĘųĢ唣Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½___”£
£Ø2£©ĀĖŌü1ŗĶĀĖŌü3Ö÷ŅŖ³É·ÖµÄ»ÆѧŹ½·Ö±šŹĒ___”¢____”£
£Ø3£©Š“³öŃõ»Æ²½ÖčÖŠ¼ÓČė¹żŃõ»ÆĒā·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½______”£
£Ø4£©µ÷½ŚpH²½ÖčÖŠ£¬ČÜŅŗpHµÄµ÷½Ś·¶Ī§ŹĒ____”£
£Ø5£©³ĮÄų¹ż³ĢÖŠ£¬Čōc(Ni2+)=2.0 mol/L£¬ÓūŹ¹100mLøĆĀĖŅŗÖŠµÄNi2+³ĮµķĶźČ«[c(Ni2+)£¼10-5mol/L]£¬ŌņŠčŅŖ¼ÓČėĢ¼ĖįÄĘ¹ĢĢåµÄĪļÖŹµÄĮæ×īÉŁĪŖ____mol”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĶ¼Ź¾Óė¶ŌÓ¦µÄŠšŹöĻą·ūµÄŹĒ( )
A.Ķ¼¼×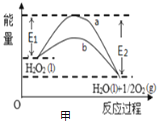 ÖŠ£¬bĒśĻßµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗH2O2(l)=H2O(l)+
ÖŠ£¬bĒśĻßµÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗH2O2(l)=H2O(l)+![]() O2(g)”÷H=(E1-E2)kJ/mol
O2(g)”÷H=(E1-E2)kJ/mol
B.Ķ¼ŅŅ ±ķŹ¾Ēā·śĖįĪŖČõĖį£¬ĒŅaµć
±ķŹ¾Ēā·śĖįĪŖČõĖį£¬ĒŅaµć![]() µÄŹżÖµ±Čbµć
µÄŹżÖµ±Čbµć![]() ŹżÖµ“ó
ŹżÖµ“ó
C.Ķ¼±ū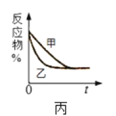 ±ķŹ¾Ń¹Ēæ¶ŌæÉÄę·“Ó¦2A(g)+2B(g)
±ķŹ¾Ń¹Ēæ¶ŌæÉÄę·“Ó¦2A(g)+2B(g)![]() 3C(g)+D(s)µÄÓ°Ļģ£¬ŅŅµÄŃ¹Ēæ±Č¼×µÄŃ¹Ēæ“ó
3C(g)+D(s)µÄÓ°Ļģ£¬ŅŅµÄŃ¹Ēæ±Č¼×µÄŃ¹Ēæ“ó
D.Ķ¼¶”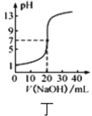 ±ķŹ¾
±ķŹ¾![]() ČÜŅŗµĪ¶Ø
ČÜŅŗµĪ¶Ø![]() “×ĖįČÜŅŗµÄµĪ¶ØĒśĻß
“×ĖįČÜŅŗµÄµĪ¶ØĒśĻß
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĪĀ¶ČŹ±£¬AgCl(s)=Ag£«(aq)£«Cl£(aq)ŌŚĖ®ÖŠµÄ³ĮµķČܽāĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©

A. ¼ÓČėAgNO3æÉŅŌŹ¹ČÜŅŗÓÉcµć±äµ½dµć
B. ¼ÓČė¹ĢĢåNaCl£¬ŌņAgClµÄČܽā¶Č¼õŠ”£¬KspŅ²¼õŠ”
C. dµćÓŠAgCl³ĮµķÉś³É
D. aµć¶ŌÓ¦µÄKspŠ”ÓŚbµć¶ŌÓ¦µÄKsp
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com