
ij��ѧ��ȤС���ú�����������ͭ�ĺϽ���ȡ�������Ȼ�����Һ���̷�����͵������壬��̽����ҵ���ϵ������á���ʵ�鷽�����£�
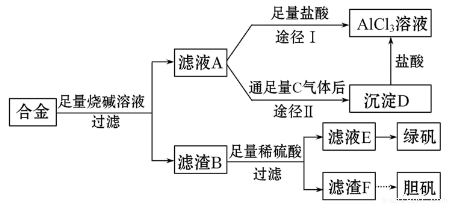
�Իش��������⣺
��1�������õ�����������ֽ������̨����Ȧ���ձ�����Ҫ����IJ���������_______________��
��2������ҺA�Ƶ�AlCl3��Һ��;����͢�����������Ϊ��������_____________��
��3������ҺE�еõ��̷������ʵ�������_______________________________��
��4��д��������F�Ʊ���������Ļ�ѧ����ʽ_____________________________��
��5����ͬѧ����ɽ�����������ܽ�Ͻ���ռ�������ᣬ������Ʒ�����Ҳ���Ƶ��������ʣ�����Ϊ���ߵķ����Ƿ��������________��������___________��
��1��©����������
��2��;����
��3������Ũ������ȴ�ᾧ
��4��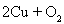
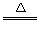
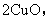
CuO+H2SO4=CuSO4+H2O��
CuSO4+5H2O=CuSO4��5H2O���𰸲�Ωһ���������ɣ�
��5�������� ��Ϊ�÷���������ʵ�鷽����Ƶļ�Լ��ԭ����������ࡢ�����Լ�������ʱ�䳤
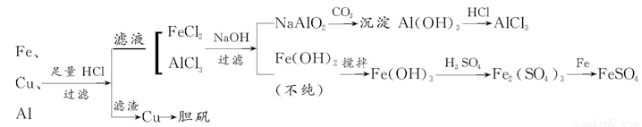
����������1���������װ�ó�����������֪�貹��IJ���������©���Ͳ���������2��������֪��ҺAΪNaAlO2��Һ������;����������ӦNaAlO2+4HCl=NaCl+AlCl3+2H2O������AlCl3��Һ�лẬ�д���NaCl���ʣ�����;����ʱ��NaAlO2+CO2+2H2O=Al��OH��3��+NaHCO3�����˵ô���Al��OH��3��Al��OH��3+3HCl=AlCl3+3H2O������AlCl3�������ʣ��ʺ�����;��Ϊ��3������BΪFe��Cu������ϡ���ᷴӦ��������ҺΪFeSO4������ΪCu������Һ����Ũ������ȴ�ᾧ���ɵ��̷�����4����Cu�Ʊ�����һ�㾭�����¼�����Ӧ��
2Cu+O2=2CuO��
CuO+H2SO4=CuSO4+H2O��
CuSO4+5H2O=CuSO4��5H2O��
��5������ͬѧ�ķ����辭���µ�ת����
��Ȼ��������࣬�����Լ�����������ʱ�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר���� ��ѧ���ü�����������ۺ�Ӧ����ϰ���������棩 ���ͣ�ѡ����
�����ӵ�������ֵ������NA��ʾ������˵������ȷ���� (����)��
A��P4O6�ķ��ӽṹ��ֻ���е�������ÿ��ԭ�ӵ�����㶼����8���ӽṹ����1 mol�÷����к��еĹ��ۼ���Ŀ��12NA
B��28 g������4 g����������ԭ����Ŀ��ȣ���ΪNA��
C��7.8 g Na2S��Na2O2�Ļ�����к��е�������������0.1NA��С��0.2NA
D��Fe��ˮ�����ڼ��������·�Ӧ������1 mol H2����ת�Ƶ��ӵ���ĿΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿���ʱ����10������ϩ��úʯ����Ȼ�����ۺ�������ϰ���������棩 ���ͣ�ѡ����
���л�����ķ����У�����ԭ�Ӷ�����ͬһƽ�����( )
A.����B���ױ�C������D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ����9-2���ؽ����绯ѧ��ʴ�������ϰ���������棩 ���ͣ������
����������й�������Һ���ʱ�ı仯�����
(1)��ʯī���缫������ͼװ�õ��AlCl3��Һ���������������ݣ��������г������ɡ�������⣬��������������Һ�л��ɹ۲쵽�������� �����ʹ���������ӷ���ʽ�� ��

(2)����ʯī���缫���NaCl��Al2(SO4)3�Ļ����Һ�������Һ�ж��ߵ����ʵ���Ũ�ȷֱ�Ϊ3 mol��L-1��0.5 mol��L-1�������б�ʾ�����̵�������ȷ���� ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ����9-2���ؽ����绯ѧ��ʴ�������ϰ���������棩 ���ͣ�ѡ����
��ͼ��ģ��绯ѧ��Ӧװ��ͼ������˵����ȷ����( )

A������K����N���������缫�ĵ缫��ӦʽΪ��Fe��2e-=Fe2��
B������K����N�������Լ������ĸ�ʴ
C������K����M���������缫�ĵ缫��ӦʽΪ�� 2Cl����2e-=Cl2��
D������K����M�������Ӵ�̼��������K��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ����3-4����������; ��������������ϰ���������棩 ���ͣ�ѡ����
��95 g����ijһ���Ȼ������ʵ��Ȼ�þ��ĩ����ˮ��������AgNO3��Һ��Ӧ������300 g AgCl����������Ȼ�þ�е����ʿ����ǣ� ��
A��NaCl B��AlCl3 C��KCl D��CaCl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ����3-4����������; ��������������ϰ���������棩 ���ͣ�ѡ����
����˵���в���ȷ���ǣ� ��
A���ҹ���ʷ��ʹ������ĺϽ�����ͭ
B��˾ĸ�춦���ҹ�Ŀǰ�ѷ��ֵ����ص���ͭ��
C��Ŀǰ������ʹ�������ĺϽ������Ͻ�
D��Ŀǰ��������;���ĺϽ��Ǹ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ���� 8-4���ܵ���ʵ��ܽ�ƽ����ϰ���������棩 ���ͣ�ѡ����
�����Ա����ж���ҽԺ�г������ᱵ���ֱ�����Ϊ�ڷ���Ӱ����ҽԺ���ȱ������ж�����ʱ���������⣬����Ҫ���ж���θ�й�����������Һ��
��֪��Ksp(BaCO3)=5.1��10��9��Ksp(BaSO4)=1.1��10��10
�����ƶ���ȷ����( )
A.����̼�ᱵ��Ϊ�ڷ���Ӱ��������ΪKsp(BaCO3)��Ksp(BaSO4)
B.���ȱ������ж�����ʱ����û�������ƣ�������̼������Һ����
C��������c(Ba2��)=1.0��10��5 mol/L����Һʱ�������������ж�
D.������0.36 mol/L��Na2SO4��Һ���������ж�����ϴθ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿��ܸ�ϰ��ʱ���� 8-1������ʵĵ�����ϰ���������棩 ���ͣ�ѡ����
���й��ڵ������Һ��������ȷ����( )
A.�����£���0.1 mol��L-1һԪ��BOH��Һ��pH=10������֪BOH��Һ���ڣ�BOH B++OH-
B++OH-
B.�����£�pH��7��NH4Cl�백ˮ�Ļ����Һ�У�c(Cl-)��c(NH4+)��c(H+)��c(OH-)
C.�к�pH���������ͬ������ʹ�����Һ������NaOH�����ʵ�����ͬ
D.��pH��4������ϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com