
【题目】下列关于反应能量的说法正确的是( )
A.Zn(s)+CuSO4(aq)=ZnSO4(aq)+Cu(s);△H =-216kJ/mol,E反应物>E生成物
B.CaCO3(s)=CaO(s)+CO2(g);△H =+178.5kJ/mol,E反应物>E生成物
C.HI(g) ![]() 1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
1/2H2(g)+ 1/2I2(s);△H = —26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量
D.H+(aq)+OH-(aq)=H2O(l);△H = —57.3kJ/mol,含1molNaOH水溶液与含0.5mol H2SO4的浓硫酸混合后放热57.3 kJ
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如右图所示,对该反应的推断合理的是( )
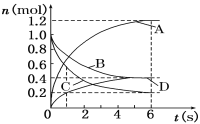
A.该反应的化学方程式为3B+4D ![]() 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】3.04 g铜镁合金完全溶解于100 mL 14.0 mol/L的浓硝酸中,得到NO2和N2O4的混合气体2240 mL(标准状况),向反应后的溶液中加入2.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到5.08 g沉淀。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2∶1
B.被还原的硝酸的物质的量是0.12 mol
C.得到5.08 g沉淀时,加入NaOH溶液的体积是700 mL
D.NO2和N2O4的混合气体中,NO2的体积分数是80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中,不正确的是( )
A.苯、乙醇和乙酸都能发生取代反应
B.液化石油气和天然气的主要成分都是甲烷
C.油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂
D.用新制的Cu(OH)2悬浊液可检验尿液中的葡萄糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某钠盐溶液中滴加稀硫酸 | 产生能使石灰水变浑浊的气体 | 该溶液一定含有CO或HCO |
B | KIO3溶液中加入HI溶液,并加入淀粉 | 溶液变蓝色 | KIO3的氧化性比I2强 |
C | 向Na2S溶液中滴加盐酸 | 产生臭鸡蛋气味的气体 | 氯的非金属性比硫的强 |
D | CO还原Fe2O3得到的黑色固体加入盐酸溶解后,再加入KSCN溶液 | 溶液不显红色 | 黑色固体中无Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸镁[ Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量 Mg(ClO3)2·6H2O 的流程如下:
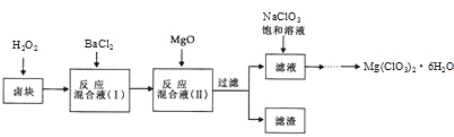
已知:①.卤块主要成分为 MgCl2·6H2O,含有 MgSO4、FeCl2等杂质。
②.四种化合物的溶解度(S)随温度(T)变化曲线 如图所示。回答下列问题:
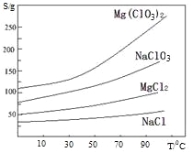
(1).过滤时主要的玻璃仪器有
(2).加入 BaCl2 的目的是除去杂质离子,检验已沉淀完全的方法是
( 3) .加入 H2O2 溶 液 的 作 用 是 : ; 加 入 MgO的 作 用是
(4).滤渣的主要成分为 。
(5).向滤液中加入 NaClO3 饱和溶液后,发生反应的化学方程式为:MgCl2+2NaClO3= Mg(ClO3)2↓+2NaCl,再进一步制取 Mg(ClO3)2·6H2O 的实 验步骤依次为① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(6).产品中 Mg(ClO3)2·6H2O 含量的测定:
步骤 1:准确称量 3.50 g 产品配成 100 mL 溶液。
步骤 2:取 10.00 mL 于锥形瓶中,加入 10.00 mL 稀硫酸和 20.00mL 1.000 mol·L-1 的 FeSO4溶液,微热。
步骤 3:冷却至室温,用 0.l000mol·L-1 K2Cr2O7 溶液滴定剩余的Fe2+至终点,
此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O
步骤 4:将步骤 2、3 重复两次,计算得平均消耗 K2Cr2O7 溶液 15.00 mL。
写出步骤 2 中发生反应的离子方程式(还原产物为Cl- )
产品中 Mg(ClO3)2·6H2O 的质量分数为【Mg(ClO3)2·6H2O 的相对分子质量为299,列出表达式即可)】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)质量比为51:32:34的NH3、CH4、H2S,其物质的量之比为 ,它们所含氢原子数之比为 ,所含质子数之比为 。
(2)在150℃,mgNH4HCO3固体完全分解生成NH3、CO2、H2O,若所得混合气体是H2密度的d倍,则用含m、d的代数式表示混合气体的物质的量为 ;用含d的代数式表示NH4HCO3的摩尔质量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.工业上电解熔融Al2O3制备金属铝
B.在海轮外壳上镶入锌块,可减缓船体的腐蚀速率
C.金属锌与稀硫酸反应制取氢气,粗锌比纯锌反应速率快
D.电解MgCl2饱和溶液,可制得金属镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com