
| A. | 锌作阳极,镀件作阴极,溶液中有锌离子 | |
| B. | 铂作阴极,镀件作阳极,溶液中有锌离子 | |
| C. | 铁作阳极,镀件作阴极,溶液中有锌离子 | |
| D. | 锌作阴极,镀件作阳极,溶液中有锌离子 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1.5g甲基(-CH3)所含有的电子数是NA | |
| B. | 14g乙烯和丙烯的混合物中含有原子的数目为NA | |
| C. | 标准状况下,1 L戊烷充分燃烧后生成的气态产物的分子数为$\frac{5}{22.4}$NA | |
| D. | 常温常压下,1mol CnH2n+2中所含有的共价键数目为(3n+1)NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸使亚氯酸的氧化性增强 | |
| B. | 溶液中的H+起催化作用 | |
| C. | 溶液中的Cl-起催化作用 | |
| D. | 逸出的ClO2使反应生成物的浓度降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生用实验室常见的酸、碱、盐和金属为反应物,并利用一个底部有小孔的试管和一个广口瓶组装成如图所示的替代简易气体发生器的即开即停装置,该装置中装有铜丝网隔板,利用该装置可制取哪些气体H2、CO2(答2种即可);若将铜丝网隔板改为铁丝网隔板,则该装置可用于制取何种气体H2,写出反应的离子方程式2Al+2OH-+2H2O═2AlO2-+3H2↑.
某学生用实验室常见的酸、碱、盐和金属为反应物,并利用一个底部有小孔的试管和一个广口瓶组装成如图所示的替代简易气体发生器的即开即停装置,该装置中装有铜丝网隔板,利用该装置可制取哪些气体H2、CO2(答2种即可);若将铜丝网隔板改为铁丝网隔板,则该装置可用于制取何种气体H2,写出反应的离子方程式2Al+2OH-+2H2O═2AlO2-+3H2↑.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠溶液中通入少量SO2:2CO32-+SO2+H2O=2HCO3-+SO32- | |
| B. | Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═Fe2++I2 | |
| C. | 少量氯气通入溴化亚铁溶液中3Cl2+2Fe2++4Br-═6Cl-+2Fe3++2Br2 | |
| D. | NaHCO3溶液水解:HCO3-+H2O=H2CO3+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) |
| 乙醇 | -117.3 | 78.5 | 0.79 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | 338.0 | 1.84 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
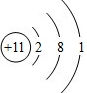 ;A、B两元素形成化合物的名称是氯化钠,用电子式表示该化合物的形成过程
;A、B两元素形成化合物的名称是氯化钠,用电子式表示该化合物的形成过程 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com