
| A£® | 0.1mol/LNa2CO3ČÜŅŗ£ŗc£ØNa+£©=2c£ØH2CO3£©+2 c£ØHCO3-£©+c£ØCO32?£© | |
| B£® | ÄÜŹ¹·ÓĢŖČÜŅŗ³ŹŗģÉ«µÄČÜŅŗ£ŗNa+”¢Ba2+”¢I-”¢NO3-æÉŅŌ“óĮæ¹²“ę | |
| C£® | ČĪŗĪĢõ¼žĻĀ£¬pH=1µÄĮņĖįČÜŅŗÖŠ£ŗc£ØH+£©=0.1mol/L | |
| D£® | ½«0.2 mol•L-1µÄHCNČÜŅŗŗĶ0.1 mol•L-1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻ£¬ČÜŅŗĻŌ¼īŠŌ£¬Ōņc£ØHCN£©=c£ØCN-£©=c£ØNa+£© |
·ÖĪö A”¢øł¾ŻĪļĮĻŹŲŗ楓·ÖĪö£»
B”¢ÄÜŹ¹·ÓĢŖČÜŅŗ³ŹŗģÉ«µÄČÜŅŗĻŌ¼īŠŌ£»
C”¢ČÜŅŗÖŠc£ØH+£©=10-pHmol/L£»
D”¢½«0.2 mol•L-1µÄHCNČÜŅŗŗĶ0.1 mol•L-1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬µĆµ½ĮĖµČÅØ¶ČµÄHCNŗĶNaCNµÄ»ģŗĻČÜŅŗ£®
½ā“š ½ā£ŗA”¢0.1mol/LNa2CO3ČÜŅŗÖŠ£¬CO32?²æ·ÖĖ®½āĪŖH2CO3ŗĶHCO3-£¬øł¾ŻĪļĮĻŹŲŗćæÉÖŖ£ŗc£ØNa+£©=2c£ØH2CO3£©+2 c£ØHCO3-£©+2c£ØCO32?£©£¬¹ŹA“ķĪó£»
B”¢ÄÜŹ¹·ÓĢŖČÜŅŗ³ŹŗģÉ«µÄČÜŅŗĻŌ¼īŠŌ£¬¶ųŌŚ¼īŠŌČÜŅŗÖŠNa+”¢Ba2+”¢I-”¢NO3-æÉŅŌ“óĮæ¹²“ę£¬¹ŹBÕżČ·£»
C”¢ČÜŅŗÖŠc£ØH+£©=10-pHmol/L£¬¹ŹĪŽĀŪŌŚŹ²Ć“Ģõ¼žĻĀ£¬pH=1µÄĮņĖįČÜŅŗÖŠ£¬ĒāĄė×ÓÅØ¶Č¾łĪŖ0.1mol/L£¬¹ŹCÕżČ·£»
D”¢½«0.2 mol•L-1µÄHCNČÜŅŗŗĶ0.1 mol•L-1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£¬µĆµ½ĮĖµČÅØ¶ČµÄHCNŗĶNaCNµÄ»ģŗĻČÜŅŗ£¬ÓÉÓŚČÜŅŗĻŌ¼īŠŌ£¬ČēNaCNµÄĖ®½ā³Ģ¶Č“óÓŚHCNµÄµēĄė³Ģ¶Č£¬ŌņČÜŅŗÖŠµÄc£ØHCN£©£¾c£ØNa+£©£¾c£ØCN-£©£¬¹ŹD“ķĪó£®
¹ŹŃ”BC£®
µćĘĄ ±¾Ģāæ¼²éĮĖČÜŅŗÖŠµÄĄė×ӵĊŠĪŖ£¬Ó¦×¢ŅāµÄŹĒµ±øł¾ŻČÜŅŗµÄpHĄ“¼ĘĖćČÜŅŗÖŠĒāĄė×ÓÅØ¶ČŹ±£¬ŗĶĪĀ¶ČĪŽ¹Ų£®


 ŹĄ¼Ķ°ŁĶØĘŚÄ©½š¾ķĻµĮŠ“š°ø
ŹĄ¼Ķ°ŁĶØĘŚÄ©½š¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ѧŠ£ŌŚ×ßµĄµÄĢśĄøøĖŠĀĖ¢ŗģÉ«µÄĘį£¬ÓĶĘįĄļµÄŗģÉ«ŃÕĮĻµÄÖ÷ŅŖ³É·ÖŹĒFe2O3 | |
| B£® | ÓĆŹ³“׳żČ„²čŗųµÄĖ®¹ø£¬ŹĒĄūÓĆĮĖŹ³“×ÖŠµÄ“×ĖįµÄĖįŠŌ | |
| C£® | ¼ŅÓĆ84Ļū¶¾Ņŗ£¬ŹĒĄūÓĆĘäÖ÷ŅŖ³É·Ö“ĪĀČĖį»ņ“ĪĀČĖįŃĪµÄĒæŃõ»ÆŠŌĻū¶¾É±¾ś | |
| D£® | ŹŠĆęÉĻĻśŹŪµÄ¼ÓµāŹ³ŃĪ£¬æÉŅŌÓƵĪ¼Óµķ·ŪČÜŅŗ¼ģŃéµāµÄ“ęŌŚ£¬ĻÖĻóŹĒ±äĄ¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
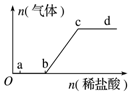 ĻņNa2CO3”¢NaHCO3»ģŗĻČÜŅŗÖŠÖšµĪµĪČėĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄĮæĖęŃĪĖį¼ÓČėĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĄė×Ó×éŌŚ¶ŌÓ¦µÄČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ£Ø””””£©
ĻņNa2CO3”¢NaHCO3»ģŗĻČÜŅŗÖŠÖšµĪµĪČėĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄĮæĖęŃĪĖį¼ÓČėĮæµÄ±ä»Æ¹ŲĻµČēĶ¼ĖłŹ¾£¬ŌņĻĀĮŠĄė×Ó×éŌŚ¶ŌÓ¦µÄČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ£Ø””””£©| A£® | aµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗAl3+”¢H+”¢SO42-”¢NO3- | |
| B£® | bµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗCa2+”¢Na+”¢OH-”¢Cl- | |
| C£® | cµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢Ca2+”¢NO3-”¢Cl- | |
| D£® | dµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗF-”¢NO3-”¢Fe3+”¢Na+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
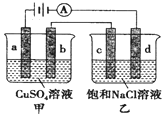
| A£® | Ļņ¼×ÖŠ¼ÓČėŹŹĮæCu£ØOH£©2£¬ČÜŅŗ×é³ÉæÉŅŌ»Öø“ | |
| B£® | µē½āŅ»¶ĪŹ±¼ä£¬ŅŅČÜŅŗÖŠ»į²śÉś°×É«³Įµķ | |
| C£® | µ±b¼«ŌöÖŲ3.2gŹ±£¬d¼«²śÉśµÄĘųĢåĢå»żĪŖ1.12L | |
| D£® | ¼×ÖŠb¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ£ŗ4OH--4e-=O2”ü+2H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 8ÖÖ | B£® | 10ÖÖ | C£® | 16ÖÖ | D£® | 20ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ąė×Ó | K+ | Mg2+ | Ca2+ | NO3- | H2PO4- | SO42- | Zn2+ |
| $\frac{ÅąŃųŅŗÅضČ}{nmol•{L}^{-1}}$ | 1 | 0.25 | 1 | 2 | 1 | 0.25 | 1 |
| A£® | Zn2+ | B£® | SO42- | C£® | Ca2+ | D£® | H2PO4- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 molµÄCH4ÖŹĮæĪŖ16g/mol | |
| B£® | 3.01”Į1023øöCO2·Ö×ÓµÄÖŹĮæŌ¼ĪŖ22g | |
| C£® | H2OµÄĦ¶ūÖŹĮæĪŖ18g | |
| D£® | ±ź×¼×“æöĻĀ£¬1 molČĪŗĪĪļÖŹĢå»ż¾łĪŖ22.4L |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com