
处于平衡状态的反应2 H2 S(g)  2H2(g)+S2(g)
2H2(g)+S2(g) 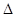 H>0,不改变其他条件的情况下合理的说法是
H>0,不改变其他条件的情况下合理的说法是
A.加入催化剂,反应途径将发生改变,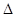 H也将随之改变 H也将随之改变 |
| B.升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C.增大压强,平衡向逆反应方向移动,将引起体系温度降低 |
| D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小 |
B
解析试题分析:A.加入催化剂,反应途径将发生改变,但是反应的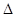 H不会改变。错误。B.升高温度,正逆反应速率都增大,对于可能反应来说,升高温度,根据平衡移动原理:化学平衡向吸热反应方向移动。由于H2S分解反应是吸热反应,所以平衡正向移动,H2S分解率增大。正确。C.该反应是个反应前后气体体积不等的反应。增大压强,化学平衡气体体积减小的反应方向即向向逆反应方向移动。由于正反应为吸热反应,所以平衡逆向移动将会引起体系温度升高。错误。D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小。压强的影响大于浓度增大的影响,根据平衡移动原理:增大压强,化学平衡向褪去体积减小的方向移动你,即向逆反应方向移动。但平衡移动的趋势是很微弱的,平衡移动只能减弱这种改变,但不能消除这种改变,因此H2的浓度不原来还是增大很多。错误。
H不会改变。错误。B.升高温度,正逆反应速率都增大,对于可能反应来说,升高温度,根据平衡移动原理:化学平衡向吸热反应方向移动。由于H2S分解反应是吸热反应,所以平衡正向移动,H2S分解率增大。正确。C.该反应是个反应前后气体体积不等的反应。增大压强,化学平衡气体体积减小的反应方向即向向逆反应方向移动。由于正反应为吸热反应,所以平衡逆向移动将会引起体系温度升高。错误。D.若体系恒容,注人一些H2后达新平衡,H2浓度将减小。压强的影响大于浓度增大的影响,根据平衡移动原理:增大压强,化学平衡向褪去体积减小的方向移动你,即向逆反应方向移动。但平衡移动的趋势是很微弱的,平衡移动只能减弱这种改变,但不能消除这种改变,因此H2的浓度不原来还是增大很多。错误。
考点:考查浓度、温度、压强、催化剂对化学反应速率及化学平衡及物质的转化率的影响的知识。


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:单选题
有关溶液中的反应3KSCN+FeCl3 Fe(SCN)3+3KCl的研究,下列说法不正确的是
Fe(SCN)3+3KCl的研究,下列说法不正确的是
| A.向平衡体系中加入少量KCl固体,溶液红色变浅 |
| B.加入少量FeCl3固体,溶液红色加深 |
| C.给体系加压,溶液红色没有明显变化 |
| D.Fe(SCN)3属于盐类,是一种弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知可逆反应:M(g)+N(g) P(g)+Q(g) △H>0 。反应达到平衡后,若要增大M的转化率,在其它条件不变的情况下可以采取的措施为( )
P(g)+Q(g) △H>0 。反应达到平衡后,若要增大M的转化率,在其它条件不变的情况下可以采取的措施为( )
①加入一定量的M ②加入一定量的N ③升高反应体系的温度 ④缩小容器体积
⑤加入某物质作催化剂 ⑥分离出一定量的P
| A.①③⑤ | B.②④⑥ | C.②③⑥ | D.④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列情况下,反应速率相同的是( )
| A.等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应 |
| B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应 |
| C.等体积等浓度HCl和CH3COOH分别与等质量的Na2CO3粉末反应 |
| D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列条件一定能使反应速率加大的是( )
①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④不断分离出生成物 ⑤加入MnO2
| A.①②③④⑤ | B.①②⑤ | C.② | D.②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
为了变废为宝,控制温室效应,工业上可用CO2来生产甲醇。一定条件下发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。
CH3OH(g)+H2O(g)。如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,下列措施中不能使c(CH3OH)增大的是 ( )。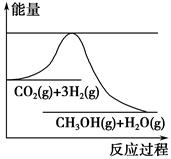
| A.降低温度 |
| B.充入He(g),使体系压强增大 |
| C.将H2O(g)从体系中分离出来 |
| D.再充入1 mol CO2和3 mol H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下,将NO2与SO2以体积比1∶2置于密闭容器中发生NO2(g)+SO2(g) SO3(g)+NO(g) ΔH="-41.8" kJ·mol-1,测得上述反应平衡时NO2与SO2体积比为1∶6,下列说法正确的是( )
SO3(g)+NO(g) ΔH="-41.8" kJ·mol-1,测得上述反应平衡时NO2与SO2体积比为1∶6,下列说法正确的是( )
| A.平衡常数K= |
| B.达到平衡后NO2与SO2的转化率相等 |
| C.SO3和NO的体积比保持不变可以证明达到平衡状态 |
| D.在反应过程中可能存在c(NO2)=c(SO2) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com