


 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
| A、Y和Z均由元素R组成,反应Y+2I-+2H+=I2+Z+H2O,其中的R元素在地壳中含量位居第一 |
| B、F2、C2H4、Na2O2、C2H6、H2O2都是含有非极性键的共价化合物 |
| C、锂钒氧化物蓄电池放电时电池的总反应式为:V2O5+Li=LixV2O5.供电时Li+向正极移动,充电时阳极的电极反应式为:LixV2O5-xe-=V2O5+xLi+ |
| D、常温下,Mg(OH)2能溶于氯化铵浓溶液的主要原因是NH4+结合OH-使沉淀溶解平衡发生移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,11.2 L氧气所含的原子数为NA |
| B、1.8 g的NH4+离子中含有的电子数为NA |
| C、常温常压下,32g O2含有的氧原子数为3NA |
| D、4.6g金属钠变为钠离子时失去的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
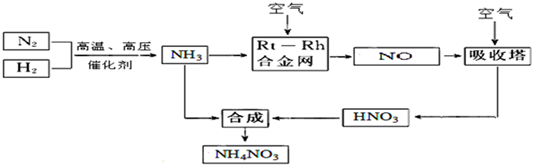
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com