
| A. | HCl | B. | KOH | C. | CaCl2 | D. | NH4 NO3 |
分析 活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,第IA族元素(H元素除外)、第IIA族和第VIA族、第VIIA族元素之间易形成离子键,据此分析解答.
解答 解:A.HCl分子中H-Cl原子之间中存在共价键,为共价化合物,故A错误;
B.KOH中钾离子和氢氧根离子之间存在离子键、O-H原子之间存在共价键,为离子化合物,故B错误;
C.氯化钙中钙离子和氯离子之间中存在离子键,为离子化合物,故C正确;
D.硝酸铵中铵根离子和硝酸根离子之间存在离子键、N-H原子及N-O原子之间存在共价键,为离子化合物,故D错误;
故选C.
点评 本题考查离子键和共价键判断,为高频考点,侧重考查基本概念,明确物质构成微粒及微粒之间作用力是解本题关键,注意不能根据是否含有金属元素判断离子键,如氯化铝为共价化合物,注意C中两个氯离子之间不存在化学键.


科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1pH为4的NaHA溶液中:c(HA-)>c(H2A)>c(A2-) | |
| B. | 向饱和氯水中加入NaOH溶液至pH=7,所得溶液中:c(Na+)>c(ClO-)>c(Cl-)>c(OH-) | |
| C. | 0.10mol•L-1 KHC2O4溶液中:c(OH-)=c(H+)+c(H2C2O4)-c(C2O42-) | |
| D. | 0.10mol•L-1Na2SO3溶液通入少量SO2:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
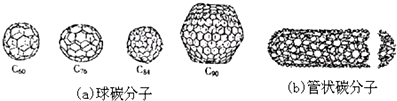
| A. | 金刚石和石墨的熔点肯定要比C60高 | |
| B. | 据估计C60熔点比金刚石和石墨要高 | |
| C. | 无论是球碳分子,还是管状碳分子、洋葱状碳分子,都应看作是碳的同素异形体 | |
| D. | C60的熔点低于C90 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该微粒的质量数为2 | |
| B. | 该微粒不显电性 | |
| C. | 它与普通中子互称为同位素 | |
| D. | 在元素周期表中与氢元素占同一位置 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
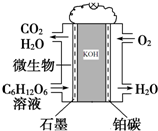 微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示:
微生物燃料电池是利用微生物作为反应主体,将有机物的化学能转化为电能.如以葡萄糖溶液为例,其工作原理如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3Cl | B. | CH2Cl2 | C. | CHCl3 | D. | CCl4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com