
【题目】铝氢化钠(NaAlH4)是有机合成的重要还原剂,其合成路线如图所示。
![]()
(1)已知AlCl3的熔点为190℃,沸点为178℃,在湖湿的空气中易水解。某实验小组利用下图中装置制备无水AlCl3。

①写出圆底烧瓶中发生反应的离子方程式:_________________。
②按气流方向连接各仪器接口,顺序为a→__________b→c→_______。 (填接口字母)
③装置F中应盛装的试剂是__________,装置D的作用是______________。
(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是______________。
(3)通过测定铝氢化钠与水反应生成氢气的体积来测定铝氢化钠样品的纯度。
①铝氢化的与水反应的化学方程式为______________。
②设计如下四种装置测定铝氢化钠样品的纯度(杂质只有氢化钠)。从简约性、准确性考虑,最恰当的装置是___(填编号)。

③某同学选用上述最恰当的裴置,称取mg铝氢化钠样品,测得生成气体的体积为VL(已折算为标准状况),重复实验操作三次,测得有关数据如下表所示,则样品中铝氢化钠的纯度为____。
实验次数 | 样品质量m(g) | 气体休积V(L) |
I | 1.20 | 1.907 |
II | 1.20 | 1.904 |
III | 1.20 | 1,901 |
【答案】 5Cl-+ClO3-+6H+=3Cl2↑+3H2O k→j→d→e h→i→f→g 饱和NaCl溶液 吸收未反应的Cl2,并防止空气中的水蒸气进入装置E中 NaH是离子化合物,难溶于有机溶剂,使反应物难以接触(或其他合理答案) NaAlH4+2H2O=NaAlO2+4H2↑ 丁 90.0%
【解析】(1)①圆底烧瓶中浓盐酸与氯酸钾反应生成氯化钾、氯气和水,发生反应的离子方程式为: 5Cl-+ClO3-+6H+=3Cl2↑+3H2O;②A装置制得氯气,通过F除去氯化氢,再通过C干燥,纯净干燥的氯气与铝粉在B中反应,产生的氯化铝在E中冷却而得,最后装置D防止空气中的水蒸气进入E。按气流方向连接各仪器接口,顺序为a→k→j→d→e →b→c→h→i→f→g;③装置F中应盛装的试剂是为了除去反应挥发出的氯化氢,为饱和NaCl溶液;装置D的作用是吸收未反应的Cl2,并防止空气中的水蒸气进入装置E中;(2)AlCl3与NaH反应时,需先将AlCl3溶于有机溶剂,再将得到的溶液滴加到NaH粉末中,此反应中NaH的转化率较低,其原因可能是NaH是离子化合物,难溶于有机溶剂,使反应物难以接触;(3) ①铝氢化的与水反应生成偏铝酸钠和氢气,反应的化学方程式为NaAlH4+2H2O=NaAlO2+4H2↑;②测定铝氢化钠的纯度,就是利用其与水反应生成氢气,测定氢气的体积,所以给的装置中丁的装置可以较准确的测定氢气的体积,所以选择丁。甲中锥形瓶中的压强变大,可能液体不能顺利流下,铝氢化钠或许不能完全反应,丙装置中导管中可能有水,使测定的气体的体积不准确,乙的操作中氢气的体积不好读数;答案选丁;③产生气体的体积平均值为![]() ,根据反应NaAlH4+2H2O=NaAlO2+4H2↑可知,样品中铝氢化钠的纯度为
,根据反应NaAlH4+2H2O=NaAlO2+4H2↑可知,样品中铝氢化钠的纯度为![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某实验小组利用FeS处理含Cu2+和Pb2+废水后的废弃固体(主要成分CuS、FeS、PbS、SiO2)制取粗铜和Fe2(SO4)3晶体,设计的操作流程如下:

(1)提高步骤①反应速率的措施,除温度外,还有_____________(写一条);
(2)处理废水时,FeS与Pb2+反应的离子方程式为____________;
(3)固体A的主要成分是_______________(填化学式);
(4)步骤⑤中,所加试剂x为____________(填标号);
a.Cl2 b.H2O2 c.KMnO4 d.HNO3
(5)检验溶液B完全转化为溶液C的试剂是_________________________;
(6)潮湿多雨的夏季,在细菌作用下,废石堆中的硫化铜与硫酸铁转化为含重金属盐的酸性废水(硫元素全部进入溶液中)而污染土壤。该转化反应的离子方程式为____________;
(7)已知,常温下FeS、CuS的Ksp分别为6.5x10-18和1.3x10-36)。现用过量的FeS处理含0.01mol·L-1 Cu2+的废水,处理后废水中c(Cu2+)=______mol·L-1(忽略体积变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:H2(g)+F2(g) === 2HF(g) △H=-270kJ/mol,下列说法正确的是( )
A. 1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B. 1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C. 在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D. 2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在10 mL 0.1 molL-1Na2CO3溶液中逐滴加入0.1 molL-1的盐酸,溶液的pH逐渐降低,此时溶液中含碳微粒的物质的量分数的变化如图所示(CO2 因逸出未画出,忽略因气体遭出而引起的溶液体积变化),下列说法正确的是
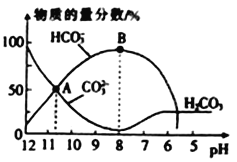
A. A点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+ c(OH-)
B. 在B点所示的溶液中,浓度最大的离子是HCO3-
C. 当熔液的pH 为7时,溶液中的阴离子只有两种
D. 已知25℃时,HCO3-的电离平衡常数Ka=5×10-11,当溶液的pH=10时,c(HCO3-)=2c(CO32-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国科学家发现,普通盐水在无线电波的照射下可燃烧。这一伟大的发现,有望解决用盐水作人类能源的重大问题。无线电频率可以降低盐水中所含元素之间的“结合力”,释放出氢原子,若点火,氢原子就会在该频率下持续燃烧。上述中的“结合力”实质是( )
A.共价键B.氢键C.分子间作用力D.离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率的说法正确的是
A. 升高温度,可以加快反应速率,缩短可逆反应达到平衡的时间
B. 化学反应达到最大限度时,正逆反应速率也达到最大且相等
C. 增加固体反应物的量可以加快反应速率
D. 用铁片和稀硫酸反应制H2比用的浓硫酸产生H2的速率慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着社会经济的发展,人们生活水平的提高和对环境要求的加强,来源广泛的高氨氮废水(主要含有NH4+)处理越来越受到重视。对于高氨氮废水的处理有多种方法。
(1)吹脱法:
![]()
使用吹脱法时需要在①中加入碱,写出发生的离子反应方程式______________________。
(2)MAP沉淀法:
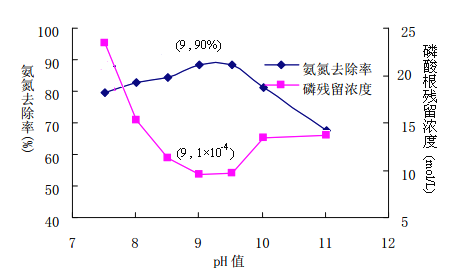
①使用化学沉淀剂处理高氨氮废水时,向高氨氮废水中投入含有Mg2+的物质和H3PO4,调节溶液pH,与NH4+反应生成MgNH4PO4(MAP)沉淀。为有效控制溶液PH,并考虑污水处理效果,则最好选用下列物质中_____。
A MgO B MgSO4 C MgCl2
②控制溶液PH的合理范围为____________________
③从溶解平衡角度解释PH过高或过低不易形成沉淀MAP的原因(已知PO43-在酸性较强条件下以HPO42-形式存在)_______________
(3)生物脱氮传统工艺:
①在有氧气的条件下,借助于好氧微生物(主要是好氧菌)的作用生成NO3-,写出反应的离子方程式_________________________。
②在无氧的酸性条件下,利用厌氧微生物(反硝化菌)的作用使NO3-与甲醇作用生成N2,达到净化水的目的。写出离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时可除去酸性废水中的硝酸盐。下列说法正确的是
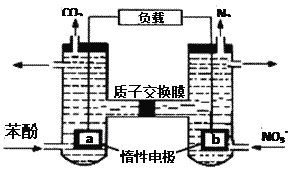
A. a极的电极反应式为C6H6O+11H2O + 28e-=6CO2↑ + 28H+
B. 外电路电子移动方向由b极到a极
C. 若正极产生5.6L气体(标况下),则转移电子2.5mol
D. 电池工作一段时间后,左池溶液的pH增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com